はじめに
褐色脂肪細胞とは、脂肪組織の一種であり、主に熱を産生する役割を持つ特殊な脂肪細胞です。新生児や冬眠動物に多く存在し、成人でも首や肩甲骨周辺などに少量見つかります。エネルギーを蓄える白色脂肪細胞とは対照的に、褐色脂肪細胞は脂肪や糖を燃焼して熱に変換することで体温維持に貢献します ( Coffee consumption may promote ‘brown fat’ function in healthy adults ) (Brown fat associated with less heart and metabolic disease | National Institutes of Health (NIH))。この高いエネルギー消費能力のため、褐色脂肪細胞は「太りにくい脂肪」あるいは「太らない脂肪」とも呼ばれ、肥満になりにくい良い脂肪として注目されています。実際、褐色脂肪は血中の糖や脂肪酸を消費して熱を作り出すため、過剰なエネルギーの蓄積を防ぎ、メタボリックシンドロームの予防に役立つ可能性が指摘されています (Brown fat associated with less heart and metabolic disease | National Institutes of Health (NIH))。
一方で、肥満ではエネルギーを蓄積する白色脂肪が過剰に増え、2型糖尿病や高血圧など様々な疾患リスクを高めることが知られています (Brown fat associated with less heart and metabolic disease | National Institutes of Health (NIH))。褐色脂肪細胞はその対極に位置し、エネルギーを消費することでこれら疾患リスクを低減する潜在力があります。近年の研究で成人にも機能的な褐色脂肪組織が存在することが明らかになり ( Brown Adipose Tissue Development and Metabolism – PMC )、肥満や糖尿病の新たな治療標的として褐色脂肪細胞への関心が高まっています ( Brown Adipose Tissue Development and Metabolism – PMC )。本記事では、褐色脂肪細胞とは何か、その特徴とエネルギー消費メカニズム、白色脂肪細胞やベージュ脂肪細胞との違い、最新の研究知見、さらに褐色脂肪細胞の活性を高める方法について、最新の研究を含めて解説します。
脂肪細胞の種類と特徴
脂肪細胞には主に白色脂肪細胞(white adipocyte)と褐色脂肪細胞(brown adipocyte)の2種類があり、加えて白色脂肪から誘導されるベージュ脂肪細胞(beige adipocyte, brite adipocyte)が存在します。それぞれ形態や役割に顕著な違いがあります。
白色脂肪細胞は体内の余剰エネルギーを中性脂肪として蓄積する貯蔵タンクのような役割を果たします。細胞内部に大きな脂肪滴を1つ蓄え、細胞核は隅に押しやられています。ミトコンドリア(細胞内の発電所)は少なく、脂肪酸を分解してATP(エネルギー通貨)を生み出す通常の代謝を行いますが、熱産生を行う脱共役タンパク質UCP1は発現していません ( Brown Adipose Tissue Development and Metabolism – PMC )。白色脂肪組織はレプチンやアディポネクチンといったホルモン(脂肪細胞から分泌されるアディポカイン)を放出し、食欲やインスリン感受性の調節など全身の代謝にも影響を与える内分泌臓器でもあります。
褐色脂肪細胞は熱を産生するために進化した脂肪細胞で、多数の小さな脂肪滴と豊富なミトコンドリアを持つ点で白色脂肪細胞と異なります ( Brown Adipose Tissue Development and Metabolism – PMC )。ミトコンドリア内には**UCP1(脱共役タンパク質1)**と呼ばれるタンパク質が高レベルで存在し、このUCP1が脂肪酸の酸化から得られるエネルギーを熱に変換することで、褐色脂肪細胞はエネルギーを放出します ( Brown Adipose Tissue Development and Metabolism – PMC )。褐色脂肪組織が褐色に見えるのは、このミトコンドリアに含まれる鉄分によるものです ( Brown Adipose Tissue Development and Metabolism – PMC )。褐色脂肪細胞は主に熱産生(非ふるえ熱産生)に特化した働きを持ち、寒冷環境下での体温維持に寄与します。また白色脂肪細胞と同様に種々のシグナル分子を分泌することから、エネルギー消費だけでなく内分泌的な役割も持つ可能性が示唆されています。
ベージュ脂肪細胞(brite脂肪細胞とも呼ばれる)は、一見白色脂肪組織の中に散在する褐色脂肪細胞のような存在です。これらはもともと白色脂肪細胞から誘導される褐色様の細胞で、寒冷刺激など特定の条件下で白色脂肪組織内に出現します ( Brown Adipose Tissue Development and Metabolism – PMC )。ベージュ脂肪細胞は形態的には褐色脂肪細胞と白色脂肪細胞の中間の特徴を示し、複数の小~中サイズの脂肪滴と比較的多くのミトコンドリアを持ち、UCP1も発現します ( Brown Adipose Tissue Development and Metabolism – PMC )。普段は白色脂肪組織に埋もれていますが、必要に応じて熱産生を担うことができるいわば「隠れた褐色脂肪細胞」です。近年、このベージュ脂肪細胞の存在が判明したことで、白色脂肪を「褐色化(ベージュ化)」することでエネルギー消費を増大させるアプローチが注目されています (Frontiers | An update on brown adipose tissue and obesity intervention: Function, regulation and therapeutic implications)。
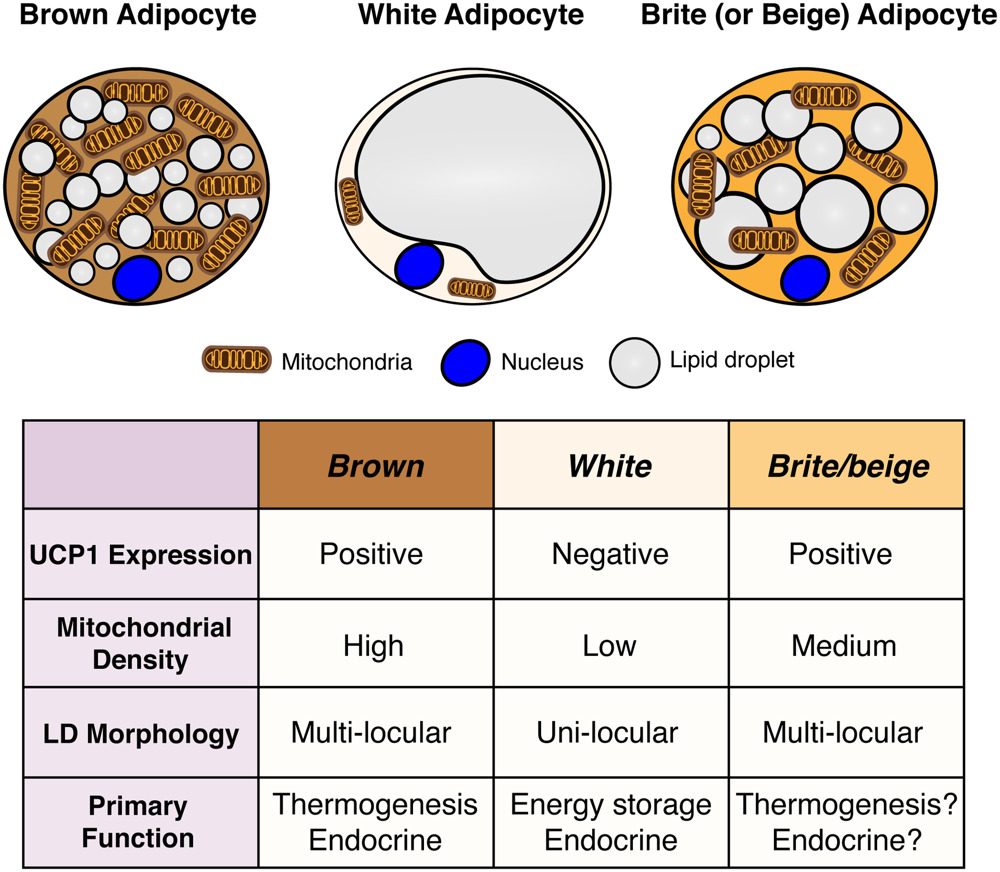
( Figure – PMC )図1: 褐色脂肪細胞、白色脂肪細胞、ベージュ脂肪細胞の構造と特徴の比較。**左:**刺激された褐色脂肪細胞は多数の小さな脂肪滴と豊富なミトコンドリアを持ち、UCP1(脱共役タンパク質1)を高発現しています。そのため脂肪酸の酸化から得られるエネルギーを熱に変換する能力が高く、ミトコンドリア中の鉄分により組織が褐色に見えます。**中央:**白色脂肪細胞は巨大な脂肪滴を1つだけ含み、ミトコンドリアは少なくUCP1を発現しません。エネルギー貯蔵が主な機能です。**右:**ベージュ脂肪細胞は白色脂肪中に誘導される褐色様細胞で、複数の脂肪滴と比較的多いミトコンドリアを持ち、UCP1を発現しています ( Brown Adipose Tissue Development and Metabolism – PMC )。
褐色脂肪細胞のエネルギー消費促進メカニズム
褐色脂肪細胞が「太らない脂肪」と呼ばれるゆえんは、その独自のエネルギー消費メカニズムにあります。最大の特徴は、ミトコンドリア内に存在するUCP1による非ふるえ熱産生です。通常、細胞は脂肪酸やブドウ糖をミトコンドリアで酸化し、そのエネルギーでATPを合成します。しかし褐色脂肪細胞では、UCP1がミトコンドリア内膜上でプロトン勾配を崩壊させ、エネルギーをATPではなく熱として放出します ( Brown Adipose Tissue Development and Metabolism – PMC )。いわば「燃料を燃やして暖房する」ような仕組みで、エネルギーが脂肪として蓄積されず熱として消費されるため、カロリー消費が促進されるのです ( Quantitative assessment of brown adipose tissue metabolic activity and volume using 18F-FDG PET/CT and β3-adrenergic receptor activation – PMC )。この過程では大量の燃料が必要となるため、褐色脂肪細胞が活性化すると血中から脂肪酸やブドウ糖が引き込まれて急速に燃焼されます ( Quantitative assessment of brown adipose tissue metabolic activity and volume using 18F-FDG PET/CT and β3-adrenergic receptor activation – PMC )。実際、褐色脂肪組織が活性化した状態では体脂肪の減少や血糖の低下が見られ、エネルギー消費臓器としての威力が示されています ( Quantitative assessment of brown adipose tissue metabolic activity and volume using 18F-FDG PET/CT and β3-adrenergic receptor activation – PMC )。
では、褐色脂肪細胞はどのようにして活性化されるのでしょうか?その鍵を握るのが交感神経から放出されるノルアドレナリン(norepinephrine)です。寒さを感じると視床下部を起点とする交感神経系が活発になり、褐色脂肪組織にノルアドレナリンが放出されます ( Brown Adipose Tissue Development and Metabolism – PMC )。褐色脂肪細胞の表面にはβ3アドレナリン受容体が存在し、ノルアドレナリンが結合すると細胞内でcAMPの増加とプロテインキナーゼA(PKA)の活性化を招きます ( Brown Adipose Tissue Development and Metabolism – PMC )。その結果、蓄えられていた中性脂肪がリパーゼによって脂肪酸とグリセロールに分解(リポリシス)され、同時にUCP1の発現量も増加します ( Brown Adipose Tissue Development and Metabolism – PMC )。脂肪分解によって生じた遊離脂肪酸はUCP1を直接活性化する作用を持ち、ミトコンドリアでの熱産生を一層促進します ( Quantitative assessment of brown adipose tissue metabolic activity and volume using 18F-FDG PET/CT and β3-adrenergic receptor activation – PMC )。この一連の流れにより、褐色脂肪細胞は寒冷下で大量の脂肪と糖を燃焼し、熱を産生して身体を温めるのです。
上述のように、従来は「褐色脂肪細胞の熱産生には脂肪分解による自前の燃料供給が不可欠」と考えられてきました。しかし最近の研究により、新たな知見も得られています。例えば、「褐色脂肪細胞内での脂肪分解が必ずしも熱産生持続の絶対条件ではない」ことが示唆されています。褐色脂肪細胞に外部から十分な脂肪酸が供給される状況であれば、細胞内の脂肪を分解しなくても熱産生が維持できる可能性があるのです ( Brown Adipose Tissue Development and Metabolism – PMC )。ただし、熱産生を駆動するUCP1を活性化するには脂肪酸が必要であるため、いずれにせよ脂肪酸(燃料)の存在は不可欠です ( Brown Adipose Tissue Development and Metabolism – PMC )。この知見は、褐色脂肪細胞が体内外の様々なエネルギー基質を柔軟に利用できることを示しており、褐色脂肪細胞によるエネルギー消費のメカニズムが想像以上に複雑で高度に制御されていることを物語っています。
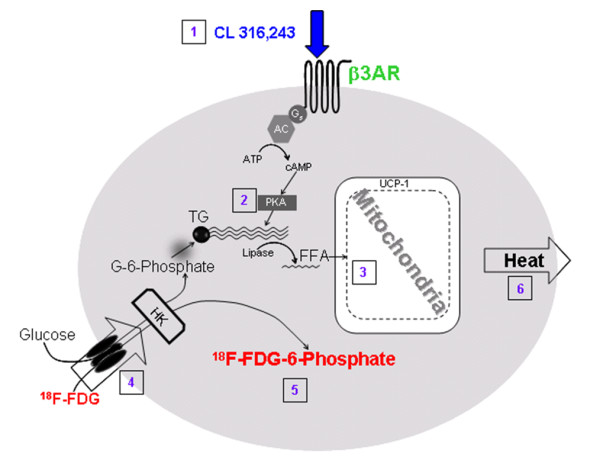
( Figure – PMC )図2: 褐色脂肪細胞の熱産生メカニズムの模式図 ( Quantitative assessment of brown adipose tissue metabolic activity and volume using 18F-FDG PET/CT and β3-adrenergic receptor activation – PMC )。ノルアドレナリンなどによって褐色脂肪細胞の表面にあるβ3アドレナリン受容体(β3AR)が活性化されると(図中①、青矢印)、細胞内でATPからcAMPへの変換が促進されアデニル酸シクラーゼやGタンパク質が活性化、プロテインキナーゼA(PKA)の作動を介してホルモン感受性リパーゼによる中性脂肪(TG)の加水分解が起こります(②) ( Quantitative assessment of brown adipose tissue metabolic activity and volume using 18F-FDG PET/CT and β3-adrenergic receptor activation – PMC )。蓄積脂肪から切り出された遊離脂肪酸(FFA)はミトコンドリア内膜のUCP1を直接活性化し(③)、ミトコンドリアで脂肪酸の酸化が亢進します。その結果、褐色脂肪細胞内の代謝活動が大幅に高まりブドウ糖の取り込みも増加します(④〜⑤) ( Quantitative assessment of brown adipose tissue metabolic activity and volume using 18F-FDG PET/CT and β3-adrenergic receptor activation – PMC )。最終的にこれら一連の反応を通じて放出されたエネルギーは熱として産生され(⑥)、体温維持や余剰エネルギーの消費に寄与します ( Quantitative assessment of brown adipose tissue metabolic activity and volume using 18F-FDG PET/CT and β3-adrenergic receptor activation – PMC )。
最新の研究動向
褐色脂肪細胞の代謝的な役割について、近年多くの研究が進み新たな知見が蓄積されています。まず、エネルギー消費と体脂肪燃焼における褐色脂肪の役割についてです。前述の通り、褐色脂肪細胞は脂肪や糖を燃料として熱に変換することで体脂肪の蓄積を抑制しうる存在です。動物実験や培養細胞の研究では、褐色脂肪細胞の活性化が脂肪蓄積を抑え体重増加を防ぐことが示されています ( Quantitative assessment of brown adipose tissue metabolic activity and volume using 18F-FDG PET/CT and β3-adrenergic receptor activation – PMC )。褐色脂肪組織はその卓越した代謝能力から「抗肥満・抗糖尿病の切り札」になり得ると期待されており ( Quantitative assessment of brown adipose tissue metabolic activity and volume using 18F-FDG PET/CT and β3-adrenergic receptor activation – PMC )、実際マウスにおける褐色脂肪の機能亢進はインスリン抵抗性の改善や脂肪減少に効果を示します ( Quantitative assessment of brown adipose tissue metabolic activity and volume using 18F-FDG PET/CT and β3-adrenergic receptor activation – PMC )。このような知見から、褐色脂肪細胞を刺激してエネルギー消費を増大させることが肥満症の治療戦略として注目されてきました (Frontiers | An update on brown adipose tissue and obesity intervention: Function, regulation and therapeutic implications)。
注目すべきは、ヒトにおける最新研究でも褐色脂肪の有用性が支持されつつある点です。2021年に発表された大規模研究では、5万例以上の成人を対象にPETスキャンで褐色脂肪の有無を調べ、褐色脂肪を持つ人と持たない人の健康指標を比較しました。その結果、褐色脂肪を持つ人は持たない人に比べて2型糖尿病、心血管疾患、心不全、脂質異常症(高コレステロール血症)や高血圧といった疾患の有病率が有意に低いことが報告されています (Brown fat associated with less heart and metabolic disease | National Institutes of Health (NIH))。興味深いことに、この傾向はBMI(体格指数)や肥満度に関係なく見られ、肥満者の中でも褐色脂肪を持つ人は持たない人より代謝疾患のリスクが低かったのです (Brown fat associated with less heart and metabolic disease | National Institutes of Health (NIH))。例えば、肥満者では褐色脂肪がない場合に約20%が2型糖尿病を抱えていましたが、褐色脂肪が存在する肥満者ではその割合が8%未満にとどまりました (Brown fat associated with less heart and metabolic disease | National Institutes of Health (NIH))。また、褐色脂肪の存在は血糖コントロールの良好さや血中脂質(トリグリセリド低値やHDLコレステロール高値)とも関連しており、褐色脂肪が全身代謝に及ぼす有益な効果が示唆されています (Brown fat associated with less heart and metabolic disease | National Institutes of Health (NIH))。以上のように、ヒトを対象とした研究からも褐色脂肪組織の活性がメタボリックヘルス(代謝の健康)に寄与しうることが支持され、褐色脂肪を増やすことが生活習慣病予防・治療につながる可能性が高まっています。
さらに、褐色脂肪細胞と糖尿病・代謝疾患との関係も盛んに研究されています。上述のような疫学的知見に加え、臨床研究では褐色脂肪を活性化することで耐糖能やインスリン感受性が改善する可能性が模索されています ( Quantitative assessment of brown adipose tissue metabolic activity and volume using 18F-FDG PET/CT and β3-adrenergic receptor activation – PMC )。褐色脂肪細胞はインスリンによってもグルコース取り込みが促進されるため、インスリン抵抗性の改善に寄与する可能性があります。また褐色脂肪組織はFGF21(繊維芽細胞増殖因子21)やネuregulin 4といったシグナル分子(いわゆる「バトカイン」BATokine)を分泌し、肝臓や筋肉など他組織の代謝を調節することも報告されています。このように褐色脂肪は単なる熱産生装置に留まらず、内分泌器官として全身のエネルギー代謝ネットワークに関与している点で、糖尿病や脂質異常症など代謝疾患の新たな制御ターゲットとなり得ます。
一方、ベージュ脂肪細胞の研究も重要なトピックです。ベージュ脂肪は白色脂肪から誘導できるため、体内の白色脂肪を「燃える脂肪」に変えてしまおうというアプローチが考えられます。動物実験では遺伝子操作や薬剤投与により白色脂肪をベージュ化することでエネルギー消費が増加し、肥満や糖尿病が改善する例が報告されています ( Capsaicin induces browning of white adipose tissue and counters obesity by activating TRPV1 channel‐dependent mechanisms – PMC )。特にIRISIN(アイリシン)やFGF21といったホルモンがベージュ脂肪誘導のキー分子として注目され、運動時に筋肉から分泌されるアイリシンが白色脂肪の褐色化(ベージュ化)を誘導することが示されています (Exercise-inducible circulating extracellular vesicle irisin promotes browning and the thermogenic program in white adipose tissue – PubMed)。この他にも様々な転写因子(例:PRDM16やPGC-1α)やシグナル経路がベージュ脂肪細胞の形成に関与することが明らかになってきており、体脂肪を燃焼しやすい性質へと変化させる方法として世界中で研究が進んでいます (Frontiers | An update on brown adipose tissue and obesity intervention: Function, regulation and therapeutic implications)。ベージュ脂肪細胞は、褐色脂肪細胞を新たに体内に増やすのと同様の効果をもたらすため、将来的には薬や食品成分で白色脂肪をベージュ化し、エネルギー消費を高めることで肥満や糖尿病に対抗するというシナリオも夢ではないかもしれません。
褐色脂肪細胞の活性を高める方法
褐色脂肪細胞の活性を高めることができれば、エネルギー消費を増やし肥満や生活習慣病の予防・改善につながる可能性があります。では、私たちは日常生活でどのようにして褐色脂肪細胞を活性化できるのでしょうか?最新の研究知見や方法をいくつか紹介します。
1. 寒冷刺激による活性化: 褐色脂肪細胞を活性化する最も古典的かつ確実な方法は寒さに身をさらすことです。人間の体は寒さを感じると褐色脂肪組織に対する交感神経刺激(ノルアドレナリン放出)を高め、熱産生を促進します ( Quantitative assessment of brown adipose tissue metabolic activity and volume using 18F-FDG PET/CT and β3-adrenergic receptor activation – PMC )。実際、一定期間寒い環境に身を置くことで身体が寒冷に順応し、褐色脂肪組織の量と活性が増加することが報告されています。ある研究では、被験者を10日間毎日寒冷環境に曝露したところ、褐色脂肪の活性が顕著に増大し、非ふるえ熱産生能力(安静時代謝に占める熱産生の割合)が向上したとされています ( JCI – Recruited brown adipose tissue as an antiobesity agent in humans )。寒冷順化により褐色脂肪組織が「鍛えられた」結果と解釈でき、日常的に軽い寒さ(例えば室温をやや低めに保つ、水風呂に入る等)に触れる習慣は褐色脂肪を刺激する一つの手段となります。ただし、過度の寒冷暴露は体調不良を招く恐れがあるため、安全かつ無理のない範囲で行うことが大切です。
2. 食事・栄養による影響: 特定の食べ物や栄養素にも褐色脂肪細胞を刺激する効果があることが研究で示唆されています。例えば、トウガラシに含まれる辛味成分カプサイシンは、痛覚・温度覚受容体であるTRPV1チャネルを活性化し、白色脂肪の褐色化(ベージュ脂肪誘導)を引き起こすことが分かっています ( Capsaicin induces browning of white adipose tissue and counters obesity by activating TRPV1 channel‐dependent mechanisms – PMC )。マウスを用いた実験では、食事にカプサイシンを添加することでエネルギー消費が増加し、高脂肪食による肥満を抑制できることが報告されました ( Capsaicin induces browning of white adipose tissue and counters obesity by activating TRPV1 channel‐dependent mechanisms – PMC )。これはカプサイシンが交感神経を刺激し、褐色脂肪およびベージュ脂肪のUCP1発現を高めた結果と考えられています。同様に、ワサビやショウガに含まれる刺激成分も一部で褐色脂肪を刺激する可能性が指摘されています。また、カフェインも褐色脂肪を活性化しうる物質として注目されています。イギリスの研究では、コーヒー1杯を飲むと褐色脂肪組織の熱産生活性が上昇することが初めてヒトで示されました ( Coffee consumption may promote ‘brown fat’ function in healthy adults )。この研究では被験者にコーヒーまたは水を摂取させ、サーモグラフィーで褐色脂肪の発熱をモニターした結果、コーヒー摂取後に首元の褐色脂肪領域の温度上昇が確認されています ( Coffee consumption may promote ‘brown fat’ function in healthy adults )。さらに培養脂肪細胞実験でもカフェインがUCP1の発現とミトコンドリア活性を高める「褐色化作用」が認められました ( Coffee consumption may promote ‘brown fat’ function in healthy adults )。これらのことから、適度なカフェイン摂取(コーヒーやお茶)や香辛料の摂取は褐色脂肪細胞の活動を後押ししうると考えられます。ただし効果には個人差があり、摂り過ぎは他の健康リスクを伴う可能性もあるため、バランスが重要です。
3. 運動とホルモンの関係: 運動そのものにもエネルギーを消費する効果がありますが、運動が褐色脂肪細胞を刺激する間接的なメカニズムにも注目が集まっています。中でも近年発見された筋肉由来のホルモンであるアイリシン(irisin)は、運動時に分泌され白色脂肪の褐色化を誘導する働きが報告されています (Exercise-inducible circulating extracellular vesicle irisin promotes browning and the thermogenic program in white adipose tissue – PubMed)。運動を継続したマウスでは血中アイリシン濃度が上昇し、白色脂肪組織でUCP1の発現増加やミトコンドリア数の増加といった「ベージュ脂肪」への変化が生じ、結果的に体重減少と耐寒能の向上が見られました (Exercise-inducible circulating extracellular vesicle irisin promotes browning and the thermogenic program in white adipose tissue – PubMed) (Exercise-inducible circulating extracellular vesicle irisin promotes browning and the thermogenic program in white adipose tissue – PubMed)。これはアイリシンが脂肪細胞に作用してAMPK経路を活性化し、UCP1依存的に熱産生を促進するためと考えられています (Exercise-inducible circulating extracellular vesicle irisin promotes browning and the thermogenic program in white adipose tissue – PubMed)。ヒトでも血中アイリシン濃度と褐色脂肪活性には関連があるとする報告があり、運動習慣が褐色脂肪を増強する一因となっている可能性があります。また運動に伴い交感神経活動が高まることも褐色脂肪刺激に寄与しうるでしょう。さらに、甲状腺ホルモンやインスリンなど他のホルモンも褐色脂肪細胞の分化・活性に影響を与えることが知られています。総じて、適度な運動を継続しホルモンバランスを整えることは、褐色脂肪細胞を含めた全身の代謝機能を高める上で有益だと考えられます。
まとめ
褐色脂肪細胞は「太らない脂肪」として、余分なエネルギーを熱として燃焼するユニークな機能を持つ脂肪細胞です。他の脂肪細胞(白色脂肪細胞やベージュ脂肪細胞)と比べても、その高いミトコンドリア量とUCP1による熱産生機構により、エネルギー消費の調節において重要な役割を果たしています。最新の研究から、褐色脂肪組織の活性が高い人ほど肥満や糖尿病、心疾患のリスクが低い傾向にあることが示され、褐色脂肪細胞を活用した新たな肥満症・代謝疾患対策への期待が高まっています (Brown fat associated with less heart and metabolic disease | National Institutes of Health (NIH))。ベージュ脂肪細胞の発見により、体内の白色脂肪を「燃える脂肪」に変える戦略も現実味を帯び始め、運動・食事・環境温度といった身近な要因で褐色脂肪を増やす取り組みも注目されています。
しかしながら、褐色脂肪細胞の活用にはまだ課題も残されています。成人の褐色脂肪の量は人によって様々であり、加齢とともに減少する傾向があります。また、褐色脂肪の活性化が因果的に体重減少や代謝改善をもたらすのか、それとも元々健康な人に褐色脂肪が多いだけなのかといった因果関係の問題も完全には解明されていません (Frontiers | An update on brown adipose tissue and obesity intervention: Function, regulation and therapeutic implications)。さらに、薬剤やその他の方法で無理に褐色脂肪を活性化した場合、過度の交感神経刺激による副作用(例えば心拍数増加や血圧上昇)のリスクも考慮する必要があります (Frontiers | An update on brown adipose tissue and obesity intervention: Function, regulation and therapeutic implications)。今後の研究では、褐色脂肪細胞を安全かつ効果的に増やす方法や、白色脂肪からの褐色化を促進する創薬・食品開発などが進められていくでしょう。また、褐色脂肪細胞の持つ内分泌的な機能や他臓器とのクロストークの解明も、新たな治療法の発見につながる可能性があります。褐色脂肪細胞は、人類が抱える肥満・糖尿病といった課題に対して大きな可能性を秘めた存在です。「太らない脂肪」を味方につけ、その機能を最大限に引き出すことができれば、私たちの健康と未来にとって大きな前進となるでしょう。
参考文献:
- Betz, M. J., & Enerbäck, S. (2018). Targeting thermogenesis in brown fat and muscle to treat obesity and metabolic disease. Nature Reviews Endocrinology, 14(2), 77-87. ( Brown Adipose Tissue Development and Metabolism – PMC ) ( Quantitative assessment of brown adipose tissue metabolic activity and volume using 18F-FDG PET/CT and β3-adrenergic receptor activation – PMC )
- Cohen, P., et al. (2021). Brown adipose tissue is associated with cardiometabolic health. Nature Medicine, 27(1), 58-65. (Brown fat associated with less heart and metabolic disease | National Institutes of Health (NIH)) (Brown fat associated with less heart and metabolic disease | National Institutes of Health (NIH))
- Fedorenko, A., Lishko, P. V., & Kirichok, Y. (2012). Mechanism of fatty-acid-dependent UCP1 uncoupling in brown fat mitochondria. Cell, 151(2), 400-413. ( Quantitative assessment of brown adipose tissue metabolic activity and volume using 18F-FDG PET/CT and β3-adrenergic receptor activation – PMC )
- Yoneshiro, T., et al. (2013). Recruited brown adipose tissue as an antiobesity agent in humans. Journal of Clinical Investigation, 123(8), 3404-3408. ( JCI – Recruited brown adipose tissue as an antiobesity agent in humans )
- Baskaran, P., et al. (2016). Capsaicin induces browning of white adipose tissue and counters obesity by activating TRPV1. British Journal of Pharmacology, 173(15), 2369-2389. ( Capsaicin induces browning of white adipose tissue and counters obesity by activating TRPV1 channel‐dependent mechanisms – PMC )
- Shi, H., et al. (2024). Exercise-inducible circulating extracellular vesicle irisin promotes browning and the thermogenic program in white adipose tissue. Acta Physiologica, 240(3), e14103. (Exercise-inducible circulating extracellular vesicle irisin promotes browning and the thermogenic program in white adipose tissue – PubMed)
- Symonds, M. E., et al. (2019). Caffeine induces browning features in adipose tissue in vitro and in vivo. Scientific Reports, 9(1), 9104. ( Coffee consumption may promote ‘brown fat’ function in healthy adults ) ( Coffee consumption may promote ‘brown fat’ function in healthy adults )
- Villarroya, J., et al. (2019). New insights into the secretory functions of brown adipose tissue. Journal of Endocrinology, 243(2), R19-R27.
- 温故知新: 脂肪組織の生理学と病態生理 (2020). 日本内分泌学会雑誌, 96(2), 123-130. (※日本語総説)