序論
私たちの体内には、休むことなく活動を続ける、驚くほど精巧でダイナミックな防御システムが存在します。それが「免疫系」です。このシステムは、国家の安全を守る諜報機関や軍隊にも似て、体内に侵入する病原体や、内部で発生した異常な細胞(がん細胞など)を常に監視し、それらが「自己(self)」の一部なのか、それとも排除すべき「非自己(non-self)」なのかを驚異的な精度で見分け、対処する能力を持っています 1。この壮大な生命維持機構の全貌を解き明かす学問が、免疫学です。
免疫システムは、大きく分けて二つの主要な部門から成り立っています。一つは、侵入者を感知すると即座に、そして広範囲にわたって対応する「自然免疫」。これは生まれながらに備わっている、いわば最前線の即応部隊です。もう一つは、特定の敵の情報を記憶し、その敵に合わせてカスタマイズされた強力な攻撃を仕掛ける「獲得免疫」。こちらは経験を積むことで強化される、精鋭の特殊部隊と言えるでしょう 3。これら二つの部門は独立して機能しているのではなく、巧みに連携し合うことで、私たちの健康を維持しています。
免疫学の進歩は、私たちの生活に計り知れない恩恵をもたらしてきました。かつて多くの命を奪った感染症を撲滅に追い込んだワクチンの開発から、現代において最も困難な病の一つであるがんの治療法に革命をもたらした新しい免疫療法まで、その影響は医療のあらゆる側面に及んでいます 6。
本稿では、この複雑で魅力的な免疫システムの世界を、基礎から最先端まで一貫して解説します。まず、自然免疫と獲得免疫という二つの防御ラインの基本的な仕組みを解き明かし、次に、T細胞やB細胞、抗体といった主要なプレイヤーたちの具体的な役割に迫ります。さらに、免疫学がどのようにして発展してきたのか、その発見と論争の歴史をたどり、研究を支える実験技術についても紹介します。最後に、がん免疫療法や腸内細菌叢(マイクロバイオーム)といった、現代医学の未来を切り拓く最新の研究動向を詳しく掘り下げます。この一冊が、生命の最も精緻な防御機構である免疫システムの理解を深めるための、信頼できる羅針盤となることを目指します。


第1部:免疫システムの基本構造 — 二つの防御ライン
免疫システムは、その応答の仕方と特性によって、大きく「自然免疫」と「獲得免疫」という二つの部門に分けられます。これらは独立したシステムではなく、互いに情報を交換し、連携することで、侵入してきた病原体に対して多層的かつ効果的な防御網を構築しています。この部では、それぞれのシステムの基本的な特徴と、両者がどのように協力して私たちの体を守っているのかを解説します。
1.1 自然免疫:生まれながらの最前線部隊
自然免疫は、私たちが生まれながらにして体に備わっている、最初の防御ラインです 1。その最大の特徴は、病原体の侵入に対して即座に反応する迅速性と、特定の病原体を区別せず、広範囲の脅威に対応する非特異性にあります。このシステムは進化の過程で古くから存在し、ヒトだけでなく、植物や昆虫など、多くの生物が同様の仕組みを持っています 1。
第一の防衛線 – 物理的・化学的バリア
病原体が体内に侵入しようとする際、まず突破しなければならないのが、物理的および化学的なバリアです。
- 物理的バリア: 体の最も外側を覆う皮膚や、消化管、呼吸器、泌尿生殖器などの内側を覆う粘膜が、最初の城壁として機能します。これらの上皮細胞は密着結合(タイトジャンクション)によって固く結びついており、病原体の物理的な侵入を阻止します 3。
- 化学的バリア: 皮膚や粘膜からは、病原体にとって過酷な環境を作り出す様々な物質が分泌されます。皮脂、唾液、涙に含まれる抗菌物質や、胃の強酸(胃酸)などがこれにあたり、微生物の増殖を抑制したり、直接破壊したりします 1。
- 微生物学的バリア: 私たちの皮膚や粘膜の表面には、膨大な数の常在細菌が生息しています。これらは一般に「マイクロバイオーム」と呼ばれ、病原性のある微生物と生息場所や栄養を奪い合ったり、抗菌物質を産生したりすることで、病原体の定着を防ぐ「生きたバリア」として機能しています 3。
第二の防衛線 – 細胞性・分子性の応答
物理的・化学的バリアを突破した病原体に対して、自然免疫は細胞と分子による迅速な応答を開始します。
- パターン認識: 自然免疫の核心的なメカニズムは、「パターン認識」です。病原体は、細菌の細胞壁成分やウイルスの核酸など、自身の生存に必須で、かつ宿主の細胞には存在しない共通の分子構造を持っています。これらは「病原体関連分子パターン(Pathogen-Associated Molecular Patterns; PAMPs)」と呼ばれます。自然免疫細胞は、「パターン認識受容体(Pattern Recognition Receptors; PRRs)」、特にトール様受容体(Toll-like receptors; TLRs)と呼ばれるセンサーを用いてこれらのPAMPsを検知します 3。これにより、過去に遭遇したことのない病原体であっても、それが「敵」であることを即座に認識できるのです 10。
- 主要な細胞: PAMPsを認識すると、以下の主要な細胞が活動を開始します。
- 食細胞(Phagocytes): マクロファージや好中球が代表的で、「貪食細胞」とも呼ばれます。これらの細胞は病原体を文字通り飲み込み(貪食)、内部で消化・分解して無力化します 8。特に好中球は、感染が起こると最初に現場に駆けつける、機動力の高い細胞です 9。
- ナチュラルキラー(NK)細胞: 自然免疫系に属する特殊なリンパ球で、ウイルスに感染した細胞やがん細胞など、表面に異常な兆候を示した自己の細胞を見つけ出し、破壊する役割を担います 1。
- マスト細胞、好塩基球、好酸球: これらの細胞も自然免疫に関与し、特にアレルギー反応や寄生虫に対する防御で重要な役割を果たします 1。
- 炎症(Inflammation): 感染部位で起こる「炎症」は、自然免疫の重要なプロセスです。活性化した免疫細胞がサイトカインやケモカインといった化学物質を放出すると、その領域の血管が拡張し、透過性が高まります。これにより、血流に乗って多くの免疫細胞や血漿成分が感染部位に集結しやすくなります。この結果生じるのが、発赤、腫脹、熱感、疼痛といった炎症の兆候です 4。
- 補体系(Complement System): 補体系は、血漿中に存在するタンパク質の一群で、他の免疫機能を「補う(complement)」ことからその名が付けられました。このシステムは連鎖的に活性化し、主に三つの重要な機能を果たします。①病原体の表面に付着して食細胞による貪食を助ける「オプソニン化」、②免疫細胞を感染部位に呼び寄せる炎症の誘発、そして③病原体の細胞膜に穴を開けて直接破壊する「膜侵襲複合体(MAC)」の形成です 8。
1.2 獲得免疫:記憶を備えた精鋭部隊
自然免疫が迅速かつ広範囲な初期対応を担うのに対し、獲得免疫はより高度に専門化された、第二の防御ラインです。その名の通り、生まれつきのものではなく、生涯を通じて病原体への曝露(感染やワクチン接種)によって「獲得」されていきます 1。
主要な特徴
- 特異性(Specificity): 獲得免疫の最大の特徴は、その驚異的な特異性です。自然免疫が病原体の共通パターンを認識するのに対し、獲得免疫は個々の病原体が持つ特定の分子、すなわち「抗原(antigen)」をピンポイントで識別します。これにより、非常に似通った病原体でさえも正確に見分けることができます 3。
- 記憶(Memory): 獲得免疫のもう一つの重要な特徴は、「免疫記憶」です。一度特定の病原体に遭遇すると、その抗原を記憶した「記憶細胞(メモリー細胞)」が体内に残ります。これにより、将来同じ病原体が再び侵入してきた際には、初回よりもはるかに迅速かつ強力な免疫応答が可能となり、多くの場合、発症を防ぐか、軽症で済ませることができます。これが、麻疹(はしか)や水痘(みずぼうそう)に一度かかると二度とかからない理由であり、ワクチンの基本原理でもあります 4。
- 応答の遅さ: 初めての病原体に対する一次応答は、適切な免疫細胞が選ばれ、増殖するまでに時間を要するため、数日から数週間かかります 1。この間、自然免疫が感染の拡大を抑える重要な役割を果たします。
主要な細胞
獲得免疫の主役は、リンパ球と呼ばれる白血球の一種です。
- B細胞(Bリンパ球): 主に「液性免疫(humoral immunity)」を担います。活性化すると、抗体(antibody)と呼ばれるタンパク質を産生し、血液や体液(古くはhumorと呼ばれた)中に放出します。この抗体が病原体や毒素に結合し、無力化します 3。
- T細胞(Tリンパ球): 主に「細胞性免疫(cell-mediated immunity)」を担います。B細胞のように抗体を放出するのではなく、細胞が直接的に機能します。感染した細胞を破壊したり、他の免疫細胞の働きを助けたり(ヘルプ)、逆に過剰な反応を抑えたり(制御)と、多様な役割を持っています 3。
表:自然免疫と獲得免疫の比較
これら二つのシステムの主な違いを以下の表にまとめます。この表は、両者の役割分担を理解するための重要な基盤となります。
| 特徴 | 自然免疫 | 獲得免疫 |
| 応答速度 | 迅速(数分〜数時間) | 遅い(数日〜数週間) |
| 特異性 | 非特異的(病原体の共通パターンを認識) | 高度に特異的(特定の抗原を認識) |
| 記憶 | なし | あり(長期的な免疫を確立) |
| 主要な細胞 | マクロファージ、好中球、NK細胞、樹状細胞 | T細胞、B細胞 |
| 主要な分子 | 補体系、サイトカイン、抗菌ペプチド | 抗体、サイトカイン |
1.3 巧みな連携プレー:自然免疫から獲得免疫へのバトンパス
自然免疫と獲得免疫は、単に時間差で働く二つの独立したシステムではありません。実際には、自然免疫が獲得免疫を起動し、その後の応答の方向性を決定づけるという、非常に緊密な連携関係にあります 3。獲得免疫が本格的に始動するまでの4日から7日間、感染の拡大を食い止めるのは自然免疫の重要な役割です 10。この連携プレーを理解することは、免疫システム全体の動態を把握する上で不可欠です。
従来、自然免疫は「非特異的で原始的な反応」、獲得免疫は「特異的で高度な反応」という二元論で語られることが多くありました 4。しかし、研究が進むにつれて、この見方は単純化しすぎていることが明らかになりました。自然免疫は単なる初期対応部隊ではなく、敵の情報を収集・分析し、その情報を基に獲得免疫という特殊部隊に出動要請と作戦指示を出す、高度な「諜報機関」兼「司令部」としての役割を担っているのです。自然免疫応答の質と種類が、その後に続く獲得免疫応答の質と種類を直接的に決定づけるため、両者は単なる連続したプロセスではなく、階層的な指揮系統の下で統合された一つの防衛戦略を形成しています 9。
伝令役 – 樹状細胞
この二つのシステム間の橋渡し役として最も重要な細胞が、「樹状細胞(dendritic cell; DC)」です。樹状細胞は、最も強力な「抗原提示細胞(Antigen-Presenting Cell; APC)」として知られています 10。
その機能は以下の通りです。
- 監視と捕捉: 樹状細胞は、皮膚や粘膜といった、外界と接する組織に広く分布し、常に周囲を監視しています。病原体が侵入してくると、それを認識して取り込みます 10。
- 抗原の処理と提示: 取り込んだ病原体を内部で分解し、その断片(抗原)を自身の細胞表面にある「MHC分子」という特別な受け皿に乗せて提示します。これは、敵の特徴を記した「手配写真」を掲げるようなものです 10。
- 移動と活性化: 病原体を捕捉すると、樹状細胞は活性化・成熟し、リンパ管を通って最も近いリンパ節へと移動します 10。
- 情報伝達: リンパ節には、まだ敵と遭遇したことのないナイーブなT細胞が多数待機しています。成熟した樹状細胞は、このT細胞に抗原を提示し、「このような敵が侵入した」という情報を伝達します。これが、自然免疫から獲得免疫への「バトンパス」の瞬間です 6。
クローン選択
樹状細胞から情報を受け取った後、獲得免疫は「クローン選択(clonal selection)」という基本原理に従って応答を開始します。この理論は、オーストラリアの科学者マクファーレン・バーネットによって提唱されました 5。
- 多様なレパートリー: 私たちの体には、それぞれが異なる一つの特定の抗原しか認識できない、膨大な種類のT細胞とB細胞が予め準備されています。この多様なリンパ球の集団を「レパートリー」と呼びます 6。
- 選択と活性化: 樹状細胞が特定の抗原を提示すると、その広大なレパートリーの中から、その抗原にぴったり合う受容体を持つT細胞だけが選択的に活性化されます 6。
- 増殖: 活性化されたT細胞は、急速に細胞分裂を繰り返し、自分と全く同じ特異性を持つ細胞の集団(クローン)を大量に作り出します。これにより、特定の敵を攻撃するための十分な数の兵士が確保されるのです 5。
このように、自然免疫による迅速な検知と情報伝達が引き金となり、獲得免疫がその特異性と記憶能力を最大限に発揮する、という一連の流れが、私たちの体を感染から守る免疫応答の根幹をなしています。
第2部:免疫の主役たち — 細胞と分子の働き
免疫システムは、多種多様な細胞と分子が織りなす複雑なネットワークです。第1部で概観した基本構造を基に、この部では、免疫応答の最前線で活躍する主要なプレイヤーたちの具体的な役割とメカニズムを、より深く掘り下げていきます。T細胞の多様な任務から、B細胞が作り出す精密な抗体、そしてシステム全体を制御する情報伝達物質まで、それぞれの専門性と連携の妙に迫ります。
2.1 T細胞の多様な任務:司令官から暗殺者まで
T細胞は、獲得免疫応答の中心的な司令塔であり、また実行部隊でもあります。その働きは非常に多岐にわたりますが、その活動の基本は、他の細胞から提示された抗原を認識することから始まります。
T細胞受容体とMHC拘束性
各T細胞は、細胞表面に「T細胞受容体(T Cell Receptor; TCR)」と呼ばれるユニークな受容体を持っています。このTCRは、特定の抗原の断片(ペプチド)を認識しますが、それだけでは反応できません。抗原ペプチドが「主要組織適合遺伝子複合体(Major Histocompatibility Complex; MHC)」と呼ばれる分子の溝に乗せられて提示された場合にのみ、それを認識して結合することができます 14。この「MHC分子とセットで抗原を認識する」という性質は「MHC拘束性」と呼ばれ、T細胞の特異性を決定づける重要な原則です。TCRの驚異的な多様性は、遺伝子断片をランダムに組み合わせる「V(D)J遺伝子再編成」という仕組みによって生み出されます 14。
MHC分子は、抗原を提示するための「ディスプレイ台」であり、主に2つのクラスが存在します。
- MHCクラスI: ほぼ全ての有核細胞の表面に存在します。この分子は、細胞の「内部」で産生されたタンパク質の断片を提示します。例えば、ウイルスに感染した細胞が作るウイルスタンパク質や、がん細胞が作る異常なタンパク質などです。これは、各細胞が「私は正常です」あるいは「私は内部に問題を抱えています」と免疫系に報告するための「自己ステータスレポート」のようなものです 1。
- MHCクラスII: 樹状細胞、マクロファージ、B細胞といった、プロの抗原提示細胞(APC)の表面にのみ存在します。この分子は、細胞が「外部」から取り込んだ病原体などのタンパク質の断片を提示します。これは、「体内に侵入者を発見した」という「敵発見レポート」の役割を果たします 6。
このMHCクラスIとクラスIIの使い分けは、免疫系が「内部の脅威」と「外部の脅威」を区別し、それぞれに適した応答戦略をとるための、非常に巧妙な仕組みです。内部の脅威(ウイルス感染細胞やがん細胞)は、その細胞ごと排除する必要があります。一方、外部の脅威(細菌など)に対しては、その病原体自体を標的とする抗体の産生や、食細胞の活性化が有効です。この役割分担は、次に述べる2種類の主要なT細胞によって実行されます。
二つの主要なT細胞系統
T細胞は、その表面に持つ分子(CDマーカー)と、認識するMHCクラスによって、大きく二つの系統に分けられます。
- 細胞傷害性Tリンパ球(CTL)またはCD8$^{+}$T細胞(キラーT細胞):
免疫系の「暗殺者」です。この細胞は、MHCクラスI分子に提示された抗原を認識します 8。ウイルスに感染した細胞やがん細胞が、その表面のMHCクラスI上に異常な抗原を提示すると、CD8$^{+}$T細胞はそれを認識し、その標的細胞に細胞死(アポトーシス)を誘導する物質を放出して、直接殺害します。これにより、問題の根源である細胞ごと、脅威を取り除くことができます。 - ヘルパーT細胞(Th)またはCD4$^{+}$T細胞(ヘルパーT細胞):
免疫系の「司令官」です。この細胞は、抗原提示細胞のMHCクラスII分子に提示された抗原を認識します 11。活性化されると、自らは直接細胞を殺害しませんが、「サイトカイン」と呼ばれる多様な情報伝達物質を産生・放出し、免疫応答全体を指揮・統制します。マクロファージをより強力な殺菌マシンに変えたり、B細胞に抗体産生を命じたりと、その指令は戦況に応じて多岐にわたります。
ヘルパーT細胞のサブタイプ
CD4$^{+}$ヘルパーT細胞は、単一の機能を持つ細胞ではありません。自然免疫系から受け取った初期情報(サイトカインの種類など)に応じて、さまざまなサブタイプに分化し、脅威の種類に最適化された「作戦計画」を実行します。
- Th1細胞: 主にウイルスや細胞内寄生細菌といった「細胞内に潜む敵」との戦いを専門とします。インターフェロンガンマ(IFN-$\gamma$)などのサイトカインを産生し、マクロファージを強力に活性化させて、取り込んだ病原体を殺す能力を高めます 2。
- Th2細胞: 主に寄生虫などの「細胞外の大きな敵」やアレルギー反応に関与します。インターロイキン4(IL-4)、IL-5、IL-13などを産生し、B細胞にIgE抗体(後述)を作らせたり、好酸球を動員したりします 2。
- Th17細胞: 主に真菌(カビ)や細胞外細菌に対する防御、特に粘膜表面での防御に重要です。IL-17というサイトカインを産生し、好中球を感染部位に集めます 14。
- 濾胞性ヘルパーT細胞(Tfh細胞): リンパ節の濾胞(B細胞が集まる領域)に存在し、B細胞が質の高い抗体(親和性が高く、クラススイッチした抗体)を産生するのを専門的に助けます 14。
- 制御性T細胞(Treg細胞): 免疫系の「平和維持部隊」です。免疫応答が過剰になり、自己の組織を攻撃してしまう「自己免疫」を防ぐために、他の免疫細胞の働きを抑制する役割を担います。免疫寛容(自己の成分に反応しない状態)の維持に不可欠な存在です 14。
このように、T細胞は脅威の種類と場所を正確に見極め、CD8$^{+}$T細胞による直接攻撃と、CD4$^{+}$T細胞の多様なサブタイプによる巧妙な指揮系統を使い分けることで、効率的かつ専門的な免疫応答を実現しているのです。
2.2 B細胞と抗体の世界:精密誘導兵器の製造工場
B細胞とそれが産生する抗体は、獲得免疫のもう一つの柱である「液性免疫」の主役です。血液や体液中をパトロールし、細胞の外にいる病原体や毒素を補足・無力化する、いわば「精密誘導兵器」の役割を果たします。
B細胞の活性化
B細胞の活性化プロセスは、T細胞の助けを借りることで、誤った攻撃を防ぐための厳密な二重チェック機構を備えています。
- 抗原の直接認識: B細胞は、自身の細胞表面にある「B細胞受容体(B Cell Receptor; BCR)」を介して、抗原を直接認識します。このBCRは、そのB細胞が将来産生する抗体と全く同じ構造を持つ、膜結合型の抗体です 14。
- T細胞による助け: 抗原を認識しただけでは、B細胞は完全には活性化されません。ほとんどの場合、活性化されたヘルパーT細胞(特にTfh細胞)からの第二のシグナル(助け)が必要です。B細胞は取り込んだ抗原を分解し、自身のMHCクラスII分子に乗せてTfh細胞に提示します。Tfh細胞が同じ抗原を認識すると、B細胞に対して活性化シグナルを送り、抗体産生を許可します。この「連携認識」により、免疫系が本当に排除すべき脅威であると確認された場合にのみ、強力な抗体応答が開始されるのです 10。
分化と抗体産生
ヘルパーT細胞からの指令を受けると、B細胞は増殖し、二つの異なるタイプの細胞へと分化します 14。
- 形質細胞(Plasma Cells): 抗体を大量に産生・分泌することに特化した「抗体産生工場」です。一つの形質細胞は、1秒間に数千個もの抗体を放出することができると言われています 11。
- 記憶B細胞(Memory B Cells): 長寿命の細胞で、体内に長期間待機します。将来、同じ抗原が再び侵入してきた際に、迅速に形質細胞へと分化し、大量の抗体を産生することで、二次応答を担います 11。
抗体の構造と機能
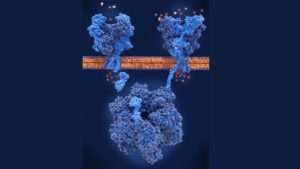
抗体(免疫グロブリン、Immunoglobulin; Ig)は、アルファベットの「Y」の字に似た特徴的な構造をしています。Yの字の二つの腕の先端部分(Fab領域)が抗原と結合する部位であり、多様な抗原に対応できるように、その構造は抗体ごとに異なります。一方、Yの字の根本部分(Fc領域)は構造が比較的共通しており、抗体のクラス(アイソタイプ)を決定し、補体系の活性化や免疫細胞との結合といった、抗体のエフェクター機能(攻撃実行機能)を担います 19。
抗体の主な機能は、高い特異性で抗原に結合し、以下のような方法で病原体を排除することです 4。
- 中和: ウイルスや毒素に結合し、それらが細胞に感染したり、害を及ぼしたりするのを物理的に阻止します。
- オプソニン化: 病原体の表面に付着し、マクロファージなどの食細胞がそれを認識しやすくするための「目印」となります。
- 補体の活性化: 抗体が病原体に結合することで、補体系(後述)の古典的経路を活性化させ、病原体の破壊を促します。
抗体のアイソタイプ(クラス)
B細胞は、免疫応答の過程で、産生する抗体のFc領域を変化させることができます。これを「クラススイッチ」と呼び、これにより、異なる機能と分布を持つ5つの主要なアイソタイプ(クラス)の抗体が作り出されます 20。
- IgM: 免疫応答の初期に最も早く産生される抗体です。五つの抗体が集まった五量体構造をしており、多数の抗原結合部位を持つため、補体系を非常に効率よく活性化させることができます 22。
- IgG: 血液中や組織液中に最も豊富に存在する抗体で、液性免疫の主役です。毒素の中和、オプソニン化、補体活性化など、多彩な機能を持ちます。また、胎盤を通過できる唯一の抗体であり、母親から胎児へと移行して、新生児を感染から守ります 21。
- IgA: 消化管や気道、涙、唾液などの粘膜分泌液中に最も多く存在する抗体です。二量体構造をとり、粘膜表面で病原体が上皮細胞に付着するのを防ぐ、最前線の防御を担います 21。
- IgE: 血中濃度は非常に低いですが、アレルギー反応や寄生虫に対する防御に重要な役割を果たします。マスト細胞や好塩基球の表面に結合し、抗原が結合するとヒスタミンなどの化学伝達物質の放出を促します 21。
- IgD: 主にナイーブB細胞の表面にBCRとして存在し、B細胞の活性化に関与していると考えられていますが、その詳細な機能はまだ完全には解明されていません 20。
2.3 サイトカインと補体系:免疫系を動かす情報伝達物質
免疫細胞たちが協調して働くためには、細胞間のコミュニケーションが不可欠です。サイトカインと補体系は、このコミュニケーションと、病原体を排除するための実行機能を担う、二つの重要な分子システムです。
サイトカイン
- 定義と機能: サイトカインは、免疫細胞(およびその他の細胞)が産生・分泌する低分子のタンパク質で、細胞間の情報伝達を担うシグナル分子です。いわば、免疫系の「公用語」であり、細胞の増殖、分化、活性化、細胞死などを制御します 10。サイトカインは非常に多様な種類が存在し、一つのサイトカインが複数の機能を持つ(多面性、pleiotropy)ことが特徴です。
- 炎症性サイトカインと抗炎症性サイトカイン: サイトカインは、その機能によって大きく二つに分類できます。
- 炎症性サイトカイン: 免疫応答を促進し、炎症を引き起こす働きをします。代表的なものに、腫瘍壊死因子(TNF-$\alpha$)、インターロイキン1(IL-1)、IL-6などがあります。これらは感染初期に産生され、免疫細胞を活性化し、感染部位に集める役割を果たします 23。
- 抗炎症性サイトカイン: 免疫応答を抑制し、過剰な炎症による組織障害を防ぐ働きをします。代表的なものに、IL-10やトランスフォーミング増殖因子ベータ(TGF-$\beta$)があります。免疫応答の終息期に重要となります 23。
健康な状態では、これら二つのバランスが適切に保たれていますが、このバランスが崩れると、自己免疫疾患やアレルギー、あるいは重篤な全身性炎症につながることがあります。 - サイトカインストーム: 免疫系の制御が効かなくなり、炎症性サイトカインが過剰に産生・放出される状態を「サイトカインストーム」と呼びます。この嵐のようなサイトカインの放出は、全身の血管や臓器に深刻なダメージを与え、生命を脅かすことがあります。敗血症や、重症のCOVID-19などで見られる現象です 23。
補体系
- カスケード反応: 補体系は、30種類以上の血漿タンパク質から構成されるシステムで、ドミノ倒しのように次々とタンパク質が活性化されていく「カスケード反応」によって機能します。この仕組みにより、最初の小さなシグナルが劇的に増幅されます 12。
- 三つの活性化経路: このカスケード反応が開始されるきっかけには、主に三つの経路があります 12。
- 古典経路(Classical Pathway): 主に、抗原に結合した抗体(特にIgGやIgM)によって活性化されます。これは、獲得免疫(抗体)が自然免疫(補体)のエフェクター機能を動員する、両システム間の重要な連携点です 12。
- レクチン経路(Lectin Pathway): 血液中のマンノース結合レクチン(MBL)というタンパク質が、細菌などの微生物表面に特有の糖鎖(マンノース)を認識して結合することで活性化されます。抗体を介さない、自然免疫独自の病原体認識メカニズムです 28。
- 副経路(Alternative Pathway): C3という中心的な補体タンパク質が自然にわずかに分解される「ティックオーバー」を起点とし、その産物が病原体の表面に直接結合することで活性化されます。抗体やレクチンを必要とせず、常に病原体の侵入を監視しています。また、古典経路やレクチン経路で生成されたC3の活性化産物によっても始動するため、全ての経路の応答を増幅する「増幅ループ」としても機能します 28。
- 共通の終着点: これら三つの経路は、異なる引き金で始まりますが、最終的には全て「C3」というタンパク質の切断へと収束します。C3が切断されて生じるC3bは、病原体表面に結合してオプソニン化を促進し、C3aは炎症を誘発します。さらにカスケードはC5の切断へと進み、C5aが強力な炎症誘発物質として働く一方、C5bはC6からC9までのタンパク質を順に呼び集め、最終的に病原体の膜に穴を開ける「膜侵襲複合体(MAC)」を形成して、細胞を溶解させます 12。
第3部:免疫学の歩み — 発見と論争の歴史
現代の私たちが享受している免疫学の知識は、一朝一夕に築かれたものではありません。それは、先人たちの鋭い観察、独創的な実験、そして時には激しい科学的論争を経て、一歩一歩積み上げられてきたものです。この部では、免疫学が一個の学問として確立されていく過程を、その歴史的なマイルストーンをたどりながら紐解いていきます。
3.1 黎明期から近代へ
初期の実践と観察
免疫という概念自体は古くから存在し、紀元前430年には古代ギリシャの歴史家トゥキディデスが、アテナイで流行した疫病において、一度回復した者は二度とかからないことを記録しています 32。科学的な理解が伴わないながらも、人々は経験的に免疫の存在を知っていました。15世紀の中国やトルコでは、天然痘患者のかさぶたを粉末にして鼻から吸引させたり、皮膚の小さな傷に植え付けたりする「人痘法(variolation)」が行われていました。これは、弱毒化された病原体によって免疫を獲得しようとする、ワクチンの原型とも言える試みでした 32。
ワクチン接種の誕生と細菌学の興隆
近代免疫学の幕開けは、1796年、イギリスの医師エドワード・ジェンナーによる種痘法の開発に始まります。ジェンナーは、牛の病気である牛痘にかかった乳搾りの女性は、致死率の高い天然痘にかからないという観察に基づき、牛痘の膿を少年に接種することで天然痘への免疫が得られることを科学的に証明しました 19。これが、人類が感染症を克服する上での大きな一歩となりました。
しかし、免疫システムが「何と」戦っているのかが明らかになるのは、19世紀後半のルイ・パスツールとロベルト・コッホの登場を待たねばなりませんでした。彼らは「細菌説」を確立し、多くの病気が目に見えない微生物によって引き起こされることを証明しました 19。敵の正体が明らかになったことで、免疫学は初めて科学的な土台を得たのです。パスツールはまた、病原体の毒性を弱める「弱毒化」という手法を開発し、狂犬病などのワクチンを実用化しました 19。
大論争:細胞性免疫 vs. 液性免疫
19世紀末から20世紀初頭にかけて、免疫学の分野では、体を守る主役が「細胞」なのか、それとも血液中の「液体成分」なのかを巡って、二つの大きな学派が対立しました。この論争は、免疫学の二つの大きな柱、すなわち自然免疫と獲得免疫の発見へとつながる、非常に生産的なものでした。
- 細胞性免疫説: ロシアの生物学者イリヤ・メチニコフが提唱しました。彼は1883年、ヒトデの幼生の実験中に、体内に侵入した異物を白血球のような細胞が取り囲んで食べてしまう現象を発見し、これを「食作用(phagocytosis)」と名付けました。メチニコフは、この食細胞こそが免疫の主役であると主張しました 19。彼の研究は、今日の自然免疫、特にマクロファージや好中球の働きの理解の基礎を築きました。
- 液性免疫説: ドイツのパウル・エールリヒとエミール・フォン・ベーリングが中心となって進めました。彼らは、ジフテリアや破傷風といった細菌が産生する毒素に対して、動物の血清(血液から血球などを取り除いた液体成分)が中和作用を持つことを発見しました。この血清中の因子を「抗毒素」、すなわち後の「抗体」であると考え、血液や体液(古くはhumorと呼ばれた)中の分子こそが免疫の主役であると主張しました 19。この研究は、獲得免疫、特にB細胞と抗体の働きの理解の礎となりました。
この論争は、メチニコフ率いるフランスのパスツール研究所と、エールリヒらのドイツ学派との間で、国家的な対立の様相さえ呈しました 37。当初は、特異的な治療法(抗血清療法)に直結した液性免疫説が優勢に見えました。しかし、最終的には、どちらか一方が正しいのではなく、両者が共に不可欠な役割を果たしていることが理解されるようになります。この偉大な功績を称え、1908年のノーベル生理学・医学賞は、メチニコフとエールリヒの二人に共同で授与されました 33。
科学の歴史は、しばしばこのような対立する理論の衝突と、その後の統合によって前進します。細胞性免疫と液性免疫の論争は、一見すると対極にある二つの考え方が、実はより大きな全体像を構成する二つの側面であったことを示す典型的な例です。一方の理論の不完全さをもう一方が補い、やがて新しい技術や発見が両者を結びつけることで、学問はより深く、より正確な理解へと至るのです。この弁証法的なプロセスこそが、免疫学を発展させてきた原動力と言えるでしょう。
3.2 ノーベル賞に輝く発見たち
20世紀を通じて、免疫学は飛躍的な発展を遂げました。その輝かしい歴史は、数々のノーベル賞受賞という形で記録されています。ここでは、免疫学の根幹をなす重要な発見を、ノーベル賞を受賞した研究を中心に時系列で紹介します。
表:免疫学における主要な発見とノーベル賞
| 年代 | 発見/出来事 | 主要な科学者 | 意義 |
| 1796 | ワクチン接種 | Edward Jenner | 天然痘に対する予防接種を科学的に実証。 |
| 1883 | 食作用 | Elie Metchnikoff | 免疫における細胞の役割を発見(細胞性免疫の基礎)。 |
| 1890 | 抗毒素(抗体) | Emil von Behring, 柴三郎 北里 | 血清中の液性因子が毒素を中和することを発見(液性免疫の基礎)。 |
| 1900 | 抗体形成の側鎖説 | Paul Ehrlich | 抗体の特異性と産生のメカニズムに関する最初の理論を提唱。 |
| 1902 | アナフィラキシー | Charles Richet, Paul Portier | 免疫応答が有害にもなりうることを発見(アレルギー研究の端緒)。 |
| 1919 | 補体系 (ノーベル賞) | Jules Bordet | 抗体の働きを助ける血清成分を発見 [39]。 |
| 1930 | ヒト血液型 (ノーベル賞) | Karl Landsteiner | 輸血を可能にした免疫学的発見 [39]。 |
| 1957 | クローン選択説 | Frank Macfarlane Burnet | 獲得免疫の特異性と記憶の基本原理を説明 [34]。 |
| 1960 | 免疫寛容 (ノーベル賞) | Frank Macfarlane Burnet, Peter Medawar | 免疫系が「自己」を攻撃しない仕組みを解明 [39]。 |
| 1958-62 | 主要組織適合遺伝子複合体(MHC) (ノーベル賞 1980) | Jean Dausset, George Snell | 移植拒絶と自己・非自己認識を司る遺伝子群を発見 [39]。 |
| 1959-62 | 抗体の化学構造 (ノーベル賞 1972) | Gerald Edelman, Rodney Porter | 抗体のY字構造と機能を解明 [34, 39]。 |
| 1974 | MHC拘束性 (ノーベル賞 1996) | Peter Doherty, Rolf Zinkernagel | T細胞が抗原をMHC分子と共に認識する仕組みを解明 [39]。 |
| 1975 | モノクローナル抗体 (ノーベル賞 1984) | Georges Köhler, César Milstein | 均一な抗体を大量生産する技術を開発 [19, 39]。 |
| 1987 | 抗体多様性の遺伝的原理 (ノーベル賞) | Susumu Tonegawa | V(D)J遺伝子再編成のメカニズムを解明 [39]。 |
| 1995 | 制御性T細胞 (ノーベル賞 2025) | Shimon Sakaguchi | 自己免疫を防ぐ抑制性のT細胞を発見 [17, 18, 41]。 |
| 2011 | 樹状細胞とTLR (ノーベル賞) | Bruce Beutler, Jules Hoffmann, Ralph Steinman | 自然免疫の活性化と獲得免疫への橋渡しのメカニズムを解明。 |
| 2018 | がん免疫療法 (ノーベル賞) | James P. Allison, Tasuku Honjo | 免疫チェックポイント阻害によるがん治療法を開発 [35]。 |
この表が示すように、免疫学の歴史は、個々の発見が積み重なるだけでなく、それらの発見が互いに結びつき、より大きな概念へと統合されていく過程でもあります。例えば、MHCの発見(1958-62年)と、T細胞がMHCと共に抗原を認識するというMHC拘束性の発見(1974年)は、細胞性免疫と液性免疫をつなぐ、T細胞中心の免疫観を確立する上で決定的な役割を果たしました。また、抗体の構造決定(1959-62年)と、その多様性がどのように遺伝的に生み出されるかの解明(1987年)は、分子レベルでの理解を飛躍的に深めました。ノーベル賞は、しばしば、このように以前は別々のものと考えられていた概念を統合し、分野全体のパラダイムを転換させた研究に与えられています。
第4部:免疫を可視化する技術 — 研究を支える実験手法
免疫学の進歩は、免疫システムの複雑な働きを観察し、測定するための革新的な実験技術の開発と密接に関わってきました。目に見えない細胞や分子の活動を「可視化」するこれらの技術なくして、現代の免疫学はありえません。この部では、免疫学研究の現場で不可欠なツールとなっている代表的な実験手法について、その原理と応用を解説します。
これらの技術の進化は、免疫学における問いの立て方そのものを変えてきました。初期の技術が血清中のタンパク質の有無といった「マクロ」な現象を捉えるものだったとすれば、その後の技術は個々の細胞の性質という「ミクロ」なレベルへ、そして現代の最先端技術は、個々の細胞内部の遺伝子発現という「ナノ」スケールの情報へと、その解像度を高めてきました。この解像度の向上が、免疫システムの多様性と複雑性の理解を深める原動力となってきたのです。
4.1 ELISA法:特定のタンパク質を検出する
ELISA(Enzyme-Linked Immunosorbent Assay)法は、特定のタンパク質(抗原や抗体など)を検出し、その量を測定するために広く用いられる、免疫学の基本的な技術です 42。
- 原理: ELISA法の基本原理は、抗原と抗体が特異的に結合する性質を利用することです。一般的に、ポリスチレン製のマイクロプレート(通常96個のウェルがある)の表面に、検出したい抗原に対する「捕捉抗体」を固定します。そこに血液や細胞培養液などのサンプルを加えると、サンプル中に目的の抗原が存在すれば、捕捉抗体に結合します。次に、酵素が標識された「検出抗体」を加えると、この抗体が抗原の別の部位に結合します。最後に、酵素の基質となる発色剤を加えると、酵素反応によって色が変化します。この色の濃さを測定することで、サンプル中の抗原の量を定量的に知ることができます 43。
- ELISA法の種類: 目的応じていくつかの形式があります。
- 直接ELISA: プレートに固定した抗原に、酵素標識した一次抗体を直接反応させる最もシンプルな方法です 43。
- 間接ELISA: プレートに固定した抗原に、まず標識のない一次抗体を反応させ、次にその一次抗体に結合する、酵素標識された二次抗体を反応させます。二次抗体が複数の一次抗体に結合できるため、シグナルが増幅され、感度が高まります 42。
- サンドイッチELISA: 捕捉抗体と検出抗体で抗原を「サンドイッチ」のように挟み込む方法です。二つの抗体が抗原の異なる部位を認識するため、非常に特異性が高く、サンプル中の抗原を定量する際に最も一般的に用いられます 43。
- 競合ELISA: サンプル中の抗原と、既知濃度の標識抗原を、プレートに固定した抗体に対して競合させる方法です。サンプル中の抗原濃度が高いほど、標識抗原の結合が阻害され、シグナルが弱くなります。これにより、抗原濃度を測定します 45。
- 応用: ELISA法は、その感度と特異性の高さから、臨床診断の現場で広く利用されています。HIVや肝炎ウイルスなどの感染症に対する抗体の検出、妊娠検査(HCGホルモンの検出)、自己免疫疾患における自己抗体の測定などがその例です。また、研究室では、サイトカインなどのタンパク質の濃度を測定するための必須のツールとなっています 44。ELISAは、サンプル全体の平均的なタンパク質量を測定する強力な手法ですが、どの細胞がそのタンパク質を産生しているのか、といった細胞レベルの情報は得られません。
4.2 フローサイトメトリー:個々の細胞を解析・分取する
フローサイトメトリーは、液体中に浮遊させた細胞集団の中から、個々の細胞の物理的・化学的特徴を高速で解析する技術です。ELISAがサンプル全体の平均値を見るのに対し、フローサイトメトリーは細胞一つひとつに焦点を当てることで、集団の不均一性を明らかにします 49。
- 原理: 特殊な液体(シース液)の流れに乗せて、細胞を一つずつレーザー光が照射されるポイントを通過させます。細胞がレーザー光に当たると、光が散乱したり、細胞に標識された蛍光色素が励起されて蛍光を発したりします。これらの光を複数の検出器で捉えることで、個々の細胞の情報を取得します 49。
- 主要な測定項目:
- 前方散乱光(Forward Scatter; FSC): 細胞の大きさに相関します。
- 側方散乱光(Side Scatter; SSC): 細胞の内部構造の複雑さ(核の形や細胞内顆粒の多さなど)に相関します。
- 蛍光: 特定の分子(例:T細胞表面のCD4やCD8)に結合する蛍光標識抗体を用いて細胞を染色することで、その分子を発現している細胞を同定し、その発現量を測定できます。
- 応用:
- 免疫細胞の表現型解析(Immunophenotyping): フローサイトメトリーの最も一般的な応用例です。血液などの複雑な細胞集団の中から、特定の表面マーカー(CDマーカーなど)を目印に、T細胞、B細胞、NK細胞といった様々な免疫細胞の亜集団を同定し、その割合や数を正確に数えることができます。例えば、HIV感染者の病状管理において、CD4$^{+}$T細胞の数をモニタリングするために不可欠な技術です 49。
- セルソーティング(FACS): Fluorescence-Activated Cell Sortingの略で、フローサイトメトリーの原理を応用し、解析した細胞を物理的に分離・回収する技術です。特定の蛍光特性を持つ細胞だけを選び出して、純粋な集団として回収することができます。これにより、希少な細胞集団を単離して、さらに詳細な解析(培養や遺伝子解析など)を行うことが可能になります 49。
- 機能解析: 細胞増殖、アポトーシス(プログラム細胞死)、細胞内でのサイトカイン産生など、細胞の動的な機能も測定することができます 47。
フローサイトメトリーの登場は、免疫学に革命をもたらしました。それまでは「リンパ球」と一括りにされていた細胞集団が、実は機能の異なる多様なサブセットから構成されていることを明らかにし、免疫システムの複雑な細胞ネットワークの解明を大きく前進させました。
4.3 シングルセル解析とマスサイトメトリー:免疫の多様性を解き明かす
従来のフローサイトメトリーでも、一度に複数のパラメータ(通常は10-20程度)を測定できますが、免疫システムのさらなる複雑性を解き明かすためには、より高次元の解析技術が求められていました。マスサイトメトリーとシングルセルRNAシーケンシング(scRNA-seq)は、その要求に応える最先端のシングルセル(単一細胞)解析技術です。これらの技術は、個々の細胞を前例のない解像度で描き出し、これまで見えなかった細胞の多様性や状態を明らかにします 54。
マスサイトメトリー(CyTOF)
- 原理: マスサイトメトリーは、フローサイトメトリーの進化版と言えます。蛍光色素の代わりに、ランタノイドなどの安定な重金属同位体を抗体に標識します。細胞は一つずつプラズマの炎の中に噴霧されて原子化され、標識されていた金属イオンが質量分析計(Time-Of-Flight Mass Spectrometer)で検出されます 54。
- 利点: 蛍光色素を用いる方法では、各色素の蛍光スペクトルが重なり合う「スペクトルオーバーラップ」という問題があり、同時に測定できる色(パラメータ)の数に限界がありました。一方、質量分析計は非常に高い分解能で金属イオンを区別できるため、この問題がほとんどありません。その結果、一度に40種類以上、場合によっては50種類以上のパラメータを単一細胞レベルで同時に測定することが可能になりました。これにより、個々の細胞の非常に詳細な「分子指紋」を取得できます 53。
- 応用: 特に、がんの腫瘍組織内に存在する多様な免疫細胞(腫瘍微小環境)の解析に威力を発揮しています。マスサイトメトリーによって、これまで知られていなかった免疫細胞の亜集団が発見されたり、がん免疫療法が効く患者と効かない患者とで、免疫細胞の状態がどのように異なるのかが詳細に明らかにされたりしています 56。
シングルセルRNAシーケンシング(scRNA-seq)
- 原理: scRNA-seqは、個々の細胞が持つ全てのメッセンジャーRNA(mRNA)を網羅的に解読する、革命的な技術です。これにより、一つひとつの細胞で、どの遺伝子が、どのくらい活発に働いているのか(遺伝子発現プロファイル)を知ることができます 55。
- 利点: マスサイトメトリーが予め選んだタンパク質の発現を見る「仮説検証型」のアプローチであるのに対し、scRNA-seqは細胞の状態を網羅的に見る「探索型」のアプローチです。これにより、全く新しい細胞の種類や、分化の途中段階にあるような一過性の細胞状態を発見したり、細胞がどのように発生・分化していくかの「発生軌跡」を推定したりすることが可能です 55。
- 応用: 免疫学の分野では、T細胞やマクロファージといった細胞が、これまで考えられていた以上に不均一な集団であることを明らかにしました。同じ種類の細胞に見えても、その内部では異なる遺伝子プログラムが動いており、異なる機能を持っていることが次々と発見されています。自己免疫疾患、線維症、そしてがんといった病態において、どのような免疫細胞が、どのように関与しているのかを解明するための強力なツールとなっています 55。
これらの高次元シングルセル解析技術は、免疫システムを「細胞集団の平均」としてではなく、「個性豊かな個々の細胞の集合体」として捉えることを可能にしました。このパラダイムシフトは、免疫学研究を新たなステージへと導き、より精密な疾患の理解と治療法の開発につながっています。
第5部:免疫学の最前線 — 疾患治療の未来
免疫学の基礎研究で得られた知見は、今や臨床の現場で革新的な治療法として結実しつつあります。特に、がん、自己免疫疾患、感染症といった難治性の疾患に対するアプローチは、免疫システムを巧みに操作するという新しい発想によって、大きな転換期を迎えています。この最終部では、現代医学で最も注目されている免疫学の応用分野、すなわち「がん免疫療法」と、その効果を左右する因子として脚光を浴びている「腸内細菌叢(マイクロバイオーム)」に焦点を当て、その最前線と未来への展望を探ります。
5.1 がん免疫療法の革命
古くから、免疫システムが体内で発生したがん細胞を認識し、排除しているという「免疫監視説」が提唱されてきました 7。がんは、この免疫システムの監視網を巧みにすり抜ける術を身につけた細胞の集団です。がん免疫療法は、このがんによってかけられたブレーキを外し、患者自身の免疫システムの力を再び解き放ってがんを攻撃させる、という画期的な治療法です 56。
免疫チェックポイント阻害剤
T細胞の活動は、過剰な反応によって自己の正常な組織を傷つけないように、精巧なアクセルとブレーキの仕組みによって制御されています。このブレーキ役を果たす分子が「免疫チェックポイント分子」です。代表的なものにCTLA-4やPD-1があります 62。多くのがん細胞は、この仕組みを逆手にとり、PD-L1という分子を自身の表面に発現させることで、攻撃に来たT細胞のPD-1に結合し、「攻撃停止」のシグナルを送って免疫から逃れます 63。
免疫チェックポイント阻害剤は、このPD-1とPD-L1(あるいはCTLA-4)の結合を阻害する抗体医薬です。この薬を投与すると、がん細胞がT細胞にかけていたブレーキが解除され、T細胞は再びがん細胞を異物として認識し、攻撃を再開します 62。この治療法は、一部のがん種において劇的な効果を示し、2018年にはその発見者であるジェームス・アリソン博士と本庶佑博士にノーベル生理学・医学賞が授与されました。
しかし、この治療法が全てのがん患者に有効なわけではありません。そのため、現在では次世代の免疫チェックポイント分子を標的とした研究が精力的に進められています。
- LAG-3: PD-1と同様に、疲弊したT細胞の表面に発現する抑制性の受容体です。特に、PD-1とLAG-3を同時に発現するT細胞は、がんへの攻撃能力が著しく低下していることが知られています。近年、LAG-3を標的とする抗体「レラトリマブ」と、PD-1阻害剤「ニボルマブ」の併用療法が、悪性黒色腫(メラノーマ)に対して承認されました。この併用療法は、PD-1阻害剤とCTLA-4阻害剤の併用療法に匹敵する効果を示しながら、重篤な副作用のリスクが低いという利点があり、新たな標準治療の一つとして期待されています 62。
- TIGIT: LAG-3と並んで、次世代の有望な標的として注目されている分子です。現在、多くの臨床試験でその有効性と安全性が検証されています 65。
個別化mRNAがんワクチン
COVID-19パンデミックにおいて、その開発と普及が劇的に加速したmRNAワクチン技術は、がん治療の分野でも大きな期待を集めています 68。がんワクチンは、がん細胞に特有の目印(抗原)を免疫系に教え込み、がんを標的とした免疫応答を誘導する治療法です。中でも「個別化mRNAがんワクチン」は、その究極形と言えます。
- 技術と個別化: がん細胞は、遺伝子変異の蓄積によって発生するため、その細胞表面には、正常な細胞にはない、患者一人ひとりに固有の異常なタンパク質(ネオアンチゲン)が発現しています。個別化mRNAがんワクチンは、まず患者のがん組織と正常組織のゲノムを解読し、その患者のがんに特有のネオアンチゲンを特定することから始まります。次に、特定された複数のネオアンチゲンの設計図(mRNA)を合成し、脂質ナノ粒子(LNP)という微小な脂質の膜に包み込んでワクチンとして製剤化します 64。
- 作用機序: このワクチンを患者に投与すると、mRNAが体内の細胞(特に抗原提示細胞)に取り込まれ、設計図通りにネオアンチゲンタンパク質が産生されます。産生されたネオアンチゲンは、抗原提示細胞によってT細胞に提示され、その患者のがん細胞だけを特異的に攻撃する強力なT細胞集団が新たに誘導・増強されます 64。
- 臨床試験の成果(mRNA-4157/V940): この分野における画期的な成果として、個別化mRNAがんワクチン「mRNA-4157(V940)」と免疫チェックポイント阻害剤「キイトルーダ®(ペムブロリズマブ)」の併用療法を検証したKEYNOTE-942試験が挙げられます。この試験は、手術で完全に切除されたものの再発リスクが高い悪性黒色腫の患者を対象に行われました。その結果、キイトルーダ単独の治療群と比較して、ワクチンを併用した群では、がんの再発または死亡のリスクが有意に低下することが示されました。2024年に発表された3年間の追跡データでも、その効果が持続していることが確認され、この治療法の有効性を強固なものとしました 64。現在、この併用療法は悪性黒色腫や肺がんなどを対象とした第3相臨床試験が進行中であり、2026年頃の薬事承認申請が期待されています 64。
この治療法の成功は、がん治療における二つの重要なパラダイムシフトを象徴しています。一つは「相乗効果と個別化」です。免疫チェックポイント阻害剤は、既存のT細胞のブレーキを「外す」治療法ですが、そもそも攻撃すべきT細胞が存在しない「冷たい腫瘍(cold tumor)」には効果が限定的でした。一方、個別化mRNAワクチンは、がんを特異的に攻撃するT細胞を新たに「作り出す」治療法です。この二つを組み合わせることで、新たに作り出されたT細胞が、ブレーキを外された状態で最大限に活躍できるという、強力な相乗効果が生まれます。これは、既製品の薬による画一的な治療から、患者一人ひとりの腫瘍の遺伝子情報に基づいた「オーダーメイド」の免疫応答を設計する、究極の個別化医療への移行を意味します。
5.2 腸内細菌叢(マイクロバイオーム)の役割
近年、免疫学における最もエキサイティングな発見の一つが、私たちの腸内に生息する膨大な数の微生物、すなわち「腸内細菌叢(マイクロバイオーム)」が、免疫システムの機能に極めて重要な影響を与えているという事実です。
- 第二のゲノムと免疫系の発達: 私たちの腸内には数百兆個もの微生物が生息しており、その遺伝情報の総量はヒトゲノムをはるかに凌駕することから「第二のゲノム」とも呼ばれています 77。体内の免疫細胞の約70-80%が腸に集中していることからもわかるように、腸は最大の免疫器官であり、腸内細菌叢と免疫系は密接な相互作用を繰り広げています 79。出生直後からの腸内細菌叢の形成プロセスは、免疫系の正常な発達と成熟、特に食物抗原などに対する「免疫寛容」の成立に不可欠です 77。出生時の分娩様式(経膣分娩か帝王切開か)や、乳児期の栄養(母乳か人工乳か)といった要因が、初期の腸内細菌叢の構成を大きく左右し、それが将来のアレルギー疾患や自己免疫疾患の発症リスクにまで影響を及ぼす可能性が指摘されています 77。
- がん免疫療法への影響: がん治療の文脈においても、腸内細菌叢の役割が大きな注目を集めています。複数の画期的な研究により、免疫チェックポイント阻害剤が効くかどうかは、患者の腸内細菌叢の構成によって大きく左右されることが明らかになりました 63。
- メカニズム: 特定の「善玉菌」とされる細菌(例えば、Akkermansia muciniphilaやBifidobacterium属など)が腸内にいると、それらが産生する代謝物などが全身の免疫系を適度に刺激し、T細胞の活性化を助け、抗腫瘍免疫応答を増強すると考えられています。一方で、特定の細菌は免疫抑制的に働き、治療効果を妨げる可能性も示唆されています 63。
- 治療への応用: この発見は、全く新しい治療戦略の可能性を開きました。食事療法、プロバイオティクス(善玉菌)の投与、あるいは健康なドナーの便を移植する「糞便微生物移植(Fecal Microbiota Transplantation; FMT)」といった手法を用いて、患者の腸内細菌叢を治療に有利な状態へと「操作」することで、がん免疫療法の効果を高めたり、これまで効果がなかった患者に効果をもたらしたりしようという試みが、現在、世界中で活発に進められています 83。
この腸内細菌叢の発見がもたらしたもう一つの重要な視点は、「宿主因子」の重要性です。がん治療の成否は、もはや「薬」と「がん」だけの関係で決まるのではなく、「患者」という宿主の内的環境、特に腸という巨大な免疫調節ハブの状態が決定的に重要である、という認識です。これは、治療のパラダイムをより複雑にしますが、同時に、食事や生活習慣といった、患者自身が介入可能な新しい治療の選択肢を提供するものでもあります。将来的には、抗がん剤や免疫療法薬と並んで、特定の食事や「薬としての細菌(bugs as drugs)」が処方される時代が来るかもしれません。
結論
本稿では、私たちの体を守る精緻な防御システムである免疫学の広大な世界を、その基本原理から歴史、研究技術、そして疾患治療の最前線に至るまで、包括的に探求してきた。その旅を通じて、いくつかの核心的なテーマが浮かび上がってくる。
第一に、免疫システムは、単純な二元論では語れない、高度に統合されたシステムであるということだ。迅速だが非特異的な「自然免疫」と、遅効性だが特異的で記憶能力を持つ「獲得免疫」は、単に二つの異なる防御ラインなのではなく、自然免疫が諜報機関として敵の情報を収集・分析し、獲得免疫という特殊部隊に的確な作戦指示を出すという、巧みな指揮系統の下で連携している。この連携の質こそが、効果的な免疫応答の鍵を握っている。
第二に、免疫システムは、驚くべき学習能力と適応能力、そして記憶能力を備えた、動的な存在であるということだ。V(D)J遺伝子再編成によって生み出される無限に近い多様性の中から、侵入してきた敵に合致するものだけを選び出して増殖させる「クローン選択」の原理は、ダーウィン的な進化のプロセスを個体内で実現しているかのようである。そして、一度経験した脅威を忘れない「免疫記憶」は、ワクチンという人類史上最も成功した医療介入の礎となった。
そして最後に、現代医学の未来は、免疫学の未来と分かちがたく結びついているということだ。がん細胞が免疫から逃れるための「ブレーキ」を解除する免疫チェックポイント阻害剤、患者一人ひとりの腫瘍の遺伝子情報に基づいて設計される個別化mRNAワクチン、そして免疫系の機能そのものを左右する腸内細菌叢の操作。これらの革新的なアプローチは、私たちが免疫システムを深く理解し、それを自在に操る能力を獲得しつつあることを示している。
私たちは今、免疫学がもたらす医療革命の黎明期にいる。シングルセル解析のようなゲノミクス技術が個々の細胞の挙動を解き明かし、mRNAのようなバイオテクノロジーが精密な介入を可能にし、マイクロバイオーム研究のようなシステム生物学が宿主と環境の相互作用を明らかにする。これらの知見が融合する時、免疫学は、がん、自己免疫疾患、感染症といった人類の長年の課題に対し、真に個別化された、そして根治を目指す医療を実現するための、最も強力な武器となるだろう。生命が数十億年かけて磨き上げてきたこの内なる防御システムの可能性を解き放つ挑戦は、まだ始まったばかりである。
引用文献
- Innate vs Adaptive Immunity: Key Differences | Technology Networks, 11月 3, 2025にアクセス、 https://www.technologynetworks.com/immunology/articles/innate-vs-adaptive-immunity-335116
- Innate and Adaptive Immunity | Request PDF – ResearchGate, 11月 3, 2025にアクセス、 https://www.researchgate.net/publication/341748718_Innate_and_Adaptive_Immunity
- The interaction of innate immune and adaptive immune system – PMC – PubMed Central, 11月 3, 2025にアクセス、 https://pmc.ncbi.nlm.nih.gov/articles/PMC11401974/
- What is the difference between innate and adaptive immunity? – Bupa UK, 11月 3, 2025にアクセス、 https://www.bupa.co.uk/newsroom/ourviews/innate-adaptive-immunity
- Summary to Chapter 1 – Immunobiology – NCBI Bookshelf, 11月 3, 2025にアクセス、 https://www.ncbi.nlm.nih.gov/books/NBK27164/
- Immunobiology – NCBI Bookshelf – NIH, 11月 3, 2025にアクセス、 https://www.ncbi.nlm.nih.gov/books/NBK10757/
- T cells, B cells and the immune system – MD Anderson Cancer Center, 11月 3, 2025にアクセス、 https://www.mdanderson.org/cancerwise/t-cells–b-cells-and-the-immune-system.h00-159465579.html
- In brief: The innate and adaptive immune systems – InformedHealth …, 11月 3, 2025にアクセス、 https://www.ncbi.nlm.nih.gov/books/NBK279396/
- Kuby Immunology, 11月 3, 2025にアクセス、 https://www.roswellpark.org/sites/default/files/thanavala_9-4-14_innate_immunity_part_1.pdf
- Principles of innate and adaptive immunity – Immunobiology – NCBI …, 11月 3, 2025にアクセス、 https://www.ncbi.nlm.nih.gov/books/NBK27090/
- Immunology for Non-Immunologists: Innate vs. Adaptive Immunity | Charles River, 11月 3, 2025にアクセス、 https://www.criver.com/eureka/immunology-non-immunologists-innate-vs-adaptive-immunity
- Complement system – Wikipedia, 11月 3, 2025にアクセス、 https://en.wikipedia.org/wiki/Complement_system
- Complement System Function – Cleveland Clinic, 11月 3, 2025にアクセス、 https://my.clevelandclinic.org/health/body/23370-complement-system
- Introduction to T and B lymphocytes – Autoimmunity – NCBI Bookshelf, 11月 3, 2025にアクセス、 https://www.ncbi.nlm.nih.gov/books/NBK459471/
- B Cells: Types and Function – Cleveland Clinic, 11月 3, 2025にアクセス、 https://my.clevelandclinic.org/health/body/24669-b-cells
- Role of B cells as antigen presenting cells – Frontiers, 11月 3, 2025にアクセス、 https://www.frontiersin.org/journals/immunology/articles/10.3389/fimmu.2022.954936/full
- Nobel Prize in Physiology or Medicine 2025 – Popular information – NobelPrize.org, 11月 3, 2025にアクセス、 https://www.nobelprize.org/prizes/medicine/2025/popular-information/
- Press release: The Nobel Prize in Physiology or Medicine 2025 – NobelPrize.org, 11月 3, 2025にアクセス、 https://www.nobelprize.org/prizes/medicine/2025/press-release/
- History_of_immunology – Bionity, 11月 3, 2025にアクセス、 https://www.bionity.com/en/encyclopedia/History_of_immunology.html
- Antibody Isotypes for Tumor Immunotherapy – PMC – NIH, 11月 3, 2025にアクセス、 https://pmc.ncbi.nlm.nih.gov/articles/PMC5649311/
- The distribution and functions of immunoglobulin isotypes – Immunobiology – NCBI – NIH, 11月 3, 2025にアクセス、 https://www.ncbi.nlm.nih.gov/books/NBK27162/
- Antibody Isotypes: IgG, IgA, IgM, IgE, and IgD Explained | Boster Bio, 11月 3, 2025にアクセス、 https://www.bosterbio.com/blog/post/antibody-isotypes-igg-iga-igm-ige-igd
- Cytokine – Wikipedia, 11月 3, 2025にアクセス、 https://en.wikipedia.org/wiki/Cytokine
- Cytokines, Chemokines and Their Receptors – Madame Curie …, 11月 3, 2025にアクセス、 https://www.ncbi.nlm.nih.gov/books/NBK6294/
- Historical Review of Cytokines – PMC – NIH, 11月 3, 2025にアクセス、 https://pmc.ncbi.nlm.nih.gov/articles/PMC3140102/
- Key Biomarkers of Immunomodulation: Complement Factors and Cytokines – Altasciences, 11月 3, 2025にアクセス、 https://www.altasciences.com/sites/default/files/2022-06/Key_Biomarkers_of_Immunomodulation.pdf
- New Insights into the Role of the Complement System in Human Viral Diseases – MDPI, 11月 3, 2025にアクセス、 https://www.mdpi.com/2218-273X/12/2/226
- Alternative Complement Pathway – Sino Biological, 11月 3, 2025にアクセス、 https://www.sinobiological.com/research/complement-system/complement-activation-alternative-pathway
- The complement system and innate immunity – Immunobiology – NCBI Bookshelf – NIH, 11月 3, 2025にアクセス、 https://www.ncbi.nlm.nih.gov/books/NBK27100/
- Distinction of early complement classical and lectin pathway activation via quantification of C1s/C1-INH and MASP-1/C1-INH complexes using novel ELISAs – Frontiers, 11月 3, 2025にアクセス、 https://www.frontiersin.org/journals/immunology/articles/10.3389/fimmu.2022.1039765/full
- The complement activation pathways: classical, alternative, and lectin… – ResearchGate, 11月 3, 2025にアクセス、 https://www.researchgate.net/figure/The-complement-activation-pathways-classical-alternative-and-lectin-pathway-The_fig1_362069400
- Molecular and Cellular Immunology/Immunology, 11月 3, 2025にアクセス、 https://njms.rutgers.edu/sgs/olc/mci/prot/2009/Session1Intro.pdf
- kuby-immunology-5ed.pdf – CCMH School of Medical Laboratory Science, 11月 3, 2025にアクセス、 https://www.ccmhmtschool.org/uploads/docs/kuby-immunology-5ed.pdf
- Timeline of immunology – Wikipedia, 11月 3, 2025にアクセス、 https://en.wikipedia.org/wiki/Timeline_of_immunology
- Immunology’s Coming of Age – Frontiers, 11月 3, 2025にアクセス、 https://www.frontiersin.org/journals/immunology/articles/10.3389/fimmu.2019.00684/full
- Cellular versus humoral immunology: A century-long dispute | Request PDF – ResearchGate, 11月 3, 2025にアクセス、 https://www.researchgate.net/publication/10782890_Cellular_versus_humoral_immunology_A_century-long_dispute
- Metchnikoff Advances the Cellular Theory of Immunity | Research Starters – EBSCO, 11月 3, 2025にアクセス、 https://www.ebsco.com/research-starters/history/metchnikoff-advances-cellular-theory-immunity
- Ehrlich and Metchnikoff Conduct Pioneering Immunity Research – EBSCO, 11月 3, 2025にアクセス、 https://www.ebsco.com/research-starters/history/ehrlich-and-metchnikoff-conduct-pioneering-immunity-research
- Nobel Prizes and the immune system – NobelPrize.org, 11月 3, 2025にアクセス、 https://www.nobelprize.org/prizes/themes/nobel-prizes-and-the-immune-system/
- The birth of immunology. III. The fate of the phagocytosis theory – PubMed, 11月 3, 2025にアクセス、 https://pubmed.ncbi.nlm.nih.gov/1733516/
- What is an ELISA? | Abcam, 11月 3, 2025にアクセス、 https://www.abcam.com/en-us/technical-resources/guides/elisa-guide/what-is-an-elisa
- The principle and method of ELISA – MBL Life Science, 11月 3, 2025にアクセス、 https://www.mblbio.com/bio/g/support/method/elisa.html
- Enzyme Linked Immunosorbent Assay – StatPearls – NCBI Bookshelf – NIH, 11月 3, 2025にアクセス、 https://www.ncbi.nlm.nih.gov/books/NBK555922/
- ELISA – Wikipedia, 11月 3, 2025にアクセス、 https://en.wikipedia.org/wiki/ELISA
- ELISA is a plate based technique used to detect and quantify peptides, antibodies, proteins and hormones. – BYJU’S, 11月 3, 2025にアクセス、 https://byjus.com/biology/elisa-technique/
- Immunological Techniques | SciTechnol, 11月 3, 2025にアクセス、 https://www.scitechnol.com/peer-review/immunological-techniques-tlXh.php?article_id=10976
- ELISA: What It Is, Purpose, Procedure & Results, 11月 3, 2025にアクセス、 https://my.clevelandclinic.org/health/articles/24990-elisa
- Overview of Flow Cytometry – Cell Signaling Technology, 11月 3, 2025にアクセス、 https://www.cellsignal.com/applications/flow-cytometry/flow-cytometry-overview
- www.iitk.ac.in, 11月 3, 2025にアクセス、 https://www.iitk.ac.in/che/PG_research_lab/pdf/resources/Flow-Cytometry-reading-material.pdf
- Flow cytometry – Wikipedia, 11月 3, 2025にアクセス、 https://en.wikipedia.org/wiki/Flow_cytometry
- Flow Cytometry Guide: Principles, Applications | Danaher Life Sciences, 11月 3, 2025にアクセス、 https://lifesciences.danaher.com/us/en/library/flow-cytometry-guide.html
- Flow cytometry in cancer diagnostics: where are we now? – Abcam, 11月 3, 2025にアクセス、 https://www.abcam.com/en-us/stories/articles/flow-cytometry-in-cancer-diagnostics-where-are-we-now
- Experimental approaches for the investigation of innate immunity – NIH, 11月 3, 2025にアクセス、 https://pmc.ncbi.nlm.nih.gov/articles/PMC5861483/
- Single-cell RNA sequencing to explore immune cell heterogeneity | Request PDF, 11月 3, 2025にアクセス、 https://www.researchgate.net/publication/318965039_Single-cell_RNA_sequencing_to_explore_immune_cell_heterogeneity
- The role of automated cytometry in the new era of cancer immunotherapy – PMC – NIH, 11月 3, 2025にアクセス、 https://pmc.ncbi.nlm.nih.gov/articles/PMC6142305/
- Systems Cancer Immunology for the Masses – NCI, 11月 3, 2025にアクセス、 https://www.cancer.gov/ccg/blog/2019/systems-cancer-immunology-for-the-masses
- Single-cell RNA Sequencing in Immunology – PMC – PubMed Central, 11月 3, 2025にアクセス、 https://pmc.ncbi.nlm.nih.gov/articles/PMC7770633/
- Single-cell RNA-sequencing reveals cellular heterogeneity and immune microenvironment characteristics between ocular adnexal mucosa-associated lymphoid lymphoma and IgG4−related ophthalmic disease – Frontiers, 11月 3, 2025にアクセス、 https://www.frontiersin.org/journals/immunology/articles/10.3389/fimmu.2025.1508559/full
- Single-Cell RNA Sequencing Reveals Cellular Heterogeneity and Microenv | JIR, 11月 3, 2025にアクセス、 https://www.dovepress.com/single-cell-rna-sequencing-reveals-cellular-heterogeneity-and-microenv-peer-reviewed-fulltext-article-JIR
- Single-cell RNA-seq reveals immune cell heterogeneity and increased Th17 cells in human fibrotic skin diseases – Frontiers, 11月 3, 2025にアクセス、 https://www.frontiersin.org/journals/immunology/articles/10.3389/fimmu.2024.1522076/full
- LAG-3 inhibitors: A new type of immunotherapy – MD Anderson Cancer Center, 11月 3, 2025にアクセス、 https://www.mdanderson.org/cancerwise/lag-3-inhibitors–a-new-type-of-immunotherapy.h00-159544479.html
- To Boost Cancer Immunotherapy’s Fighting Power, Look to the Gut, 11月 3, 2025にアクセス、 https://hms.harvard.edu/news/boost-cancer-immunotherapys-fighting-power-look-gut
- Moderna & Merck Announce 3-Year Data For mRNA-4157 (V940) in Combination With KEYTRUDA® (pembrolizumab) Demonstrated Sustained Improvement in Recurrence-Free Survival & Distant Metastasis-Free Survival Versus KEYTRUDA in Patients With High-Risk Stage III/IV Melanoma Following Complete Resection, 11月 3, 2025にアクセス、 https://www.merck.com/news/moderna-merck-announce-3-year-data-for-mrna-4157-v940-in-combination-with-keytruda-pembrolizumab-demonstrated-sustained-improvement-in-recurrence-free-survival-distant-metastasis-free-su/
- Application and Expectations for Immune Checkpoint Blockade of LAG3 and TIGIT, 11月 3, 2025にアクセス、 https://www.annualreviews.org/content/journals/10.1146/annurev-med-080222-100847
- Progress of immune checkpoint LAG-3 in immunotherapy – ResearchGate, 11月 3, 2025にアクセス、 https://www.researchgate.net/publication/344369211_Progress_of_immune_checkpoint_LAG-3_in_immunotherapy
- The World of Immunotherapy Needs More Than PD-1/PD-L1—Two of the New Kids on the Block: LAG-3 and TIGIT – MDPI, 11月 3, 2025にアクセス、 https://www.mdpi.com/2673-7523/4/3/10
- Health Technology Assessment of mRNA Vaccines: Clinical, Economic, and Public Health Implications – MDPI, 11月 3, 2025にアクセス、 https://www.mdpi.com/2076-393X/13/10/1045
- The future of mRNA vaccines beyond COVID-19 – CAS, 11月 3, 2025にアクセス、 https://www.cas.org/resources/cas-insights/future-mrna-vaccines
- Clinical advances and ongoing trials of mRNA vaccines for cancer treatment – PMC, 11月 3, 2025にアクセス、 https://pmc.ncbi.nlm.nih.gov/articles/PMC9512276/
- Current Progress and Future Perspectives of RNA-Based Cancer Vaccines: A 2025 Update, 11月 3, 2025にアクセス、 https://pmc.ncbi.nlm.nih.gov/articles/PMC12153701/
- Full article: Neoadjuvant personalized cancer vaccines: the final frontier?, 11月 3, 2025にアクセス、 https://www.tandfonline.com/doi/full/10.1080/14760584.2024.2303015
- A 3-Year Update From the mRNA-4157-P201 (KEYNOTE-942) Trial: Individualized Neoantigen Therapy mRNA-4157 (V940) Plus Pembrolizumab in Resected Melanoma – The Oncology Nurse, 11月 3, 2025にアクセス、 https://www.theoncologynurse.com/issue-archive/2024/november-2024-vol-17-no-4/a-3-year-update-from-the-mrna-4157-p201-keynote-942-trial
- Individualised neoantigen therapy mRNA-4157 (V940) plus pembrolizumab versus pembrolizumab monotherapy in resected melanoma (KEYNOTE-942): a randomised, phase 2b study – PubMed, 11月 3, 2025にアクセス、 https://pubmed.ncbi.nlm.nih.gov/38246194/
- Adjuvant mRNA-4157 Plus Pembrolizumab Prolongs RFS versus Pembrolizumab Alone in Patients with Resected High-Risk Melanoma | ESMO, 11月 3, 2025にアクセス、 https://www.esmo.org/oncology-news/adjuvant-mrna-4157-plus-pembrolizumab-prolongs-rfs-versus-pembrolizumab-alone-in-patients-with-resected-high-risk-melanoma
- INTerpath-001: Pembrolizumab with V940 (mRNA-4157) versus pembrolizumab with placebo for adjuvant treatment of high-risk stage II-IV melanoma. | Journal of Clinical Oncology – ASCO Publications, 11月 3, 2025にアクセス、 https://ascopubs.org/doi/10.1200/JCO.2024.42.16_suppl.TPS9616
- The gut microbiome and the immune system – Open Exploration Publishing, 11月 3, 2025にアクセス、 https://www.explorationpub.com/Journals/em/Article/100187
- Spooky by name, friendly by nature: microbes that keep us healthy – Gut Microbiota for Health, 11月 3, 2025にアクセス、 https://www.gutmicrobiotaforhealth.com/spooky-by-name-friendly-by-nature-microbes-that-keep-us-healthy/
- The Interplay between the Gut Microbiome and the Immune System in the Context of Infectious Diseases throughout Life and the Role of Nutrition in Optimizing Treatment Strategies – NIH, 11月 3, 2025にアクセス、 https://pmc.ncbi.nlm.nih.gov/articles/PMC8001875/
- The role of gut microbiota in immune homeostasis and autoimmunity – PubMed Central – NIH, 11月 3, 2025にアクセス、 https://pmc.ncbi.nlm.nih.gov/articles/PMC3337124/
- Defining the Relationship of Gut Microbiota, Immunity, and Cognition in Early Life—A Narrative Review – MDPI, 11月 3, 2025にアクセス、 https://www.mdpi.com/2072-6643/15/12/2642
- Development of systemic and mucosal immune responses against gut microbiota in early life and implications for the onset of allergies – Frontiers, 11月 3, 2025にアクセス、 https://www.frontiersin.org/journals/allergy/articles/10.3389/falgy.2024.1439303/full
- Role of gut microbiome in cancer immunotherapy: from predictive biomarker to therapeutic target – NIH, 11月 3, 2025にアクセス、 https://pmc.ncbi.nlm.nih.gov/articles/PMC10537950/
- The influence of the gut microbiome on cancer, immunity, and cancer immunotherapy – PMC, 11月 3, 2025にアクセス、 https://pmc.ncbi.nlm.nih.gov/articles/PMC6529202/
- Does the Microbiota Composition Influence the Efficacy of Colorectal Cancer Immunotherapy? – Frontiers, 11月 3, 2025にアクセス、 https://www.frontiersin.org/journals/oncology/articles/10.3389/fonc.2022.852194/full
- The Microbiome Modulates the Immune System to Influence Cancer Therapy – MDPI, 11月 3, 2025にアクセス、 https://www.mdpi.com/2072-6694/16/4/779
- The dual role of microbiota in cancer immunotherapy | Drug Discovery News, 11月 3, 2025にアクセス、 https://www.drugdiscoverynews.com/the-dual-role-microbiota-in-cancer-immunotherapy-15800