私たちの体は、わずか1個の受精卵からどのようにして複雑な臓器や組織を形成していくのでしょうか。発生学はその生命誕生の神秘を解き明かす重要な学問です。近年ではオルガノイド技術や幹細胞研究、クローン技術といった最新の科学が登場し、発生学の知見は再生医療など幅広い分野への応用が期待されています。本記事では、生命がどのようにして形作られるかを、基礎から最新研究まで丁寧に解説します。


発生学とは? 生命の設計図
発生学とは、受精から胎児が形成されるまでの生命の成り立ちを研究する分野です。一個の受精卵というたった一つの細胞が、細胞分裂と細胞分化を繰り返して数多くの細胞を生み出し、最終的に複雑な人体を形作っていきます (Basic Embryology)。このプロセスは親から受け継いだ染色体上の遺伝情報、いわば生命の設計図によって精密に制御されています (Basic Embryology)。発生学は、この設計図がどのように読まれ、胚が形づくられていくのかを解き明かす学問なのです。
生命の設計図であるDNAは全ての細胞で共通ですが、発生の過程では細胞ごとに活性化される遺伝子の組み合わせが変化し、それによって細胞は異なる形態・機能を獲得していきます。この細胞の分業化ともいえる現象を「細胞分化」と呼びます (〖高校生物基礎〗「ヒトの細胞とゲノムの働き」 | 映像授業のTry IT (トライイット))。発生学では、どのようにして受精卵から様々な細胞や組織が分化し、正しい位置に配置されていくのか、その仕組みを探っていきます。
受精から胚発生のメカニズム
新しい個体の発生は受精の瞬間から始まります。雌の卵子と雄の精子が出会い、一つに融合することで受精卵(接合子)が形成されます (Embryology – Cellular Division – Gastrulation – TeachMeAnatomy)。ヒトでは通常、卵管膨大部で受精が起こり、受精卵は細胞分裂を開始しながら子宮へと運ばれていきます。約1日後に最初の分裂が起こり受精卵は2細胞となり、その後も細胞は休む間もなく倍々に分裂していきます。
分裂を繰り返して細胞数が増えると、受精後3~4日ほどで桑実胚(そうじつはい)と呼ばれる16~32細胞ほどの胚の状態になります (Embryology – Cellular Division – Gastrulation – TeachMeAnatomy) (桑実胚(そうじつはい)とは? 意味や使い方 – コトバンク)。桑実胚とは外見が桑の実(マルベリー)に似ていることから名付けられたもので、内部にはまだ明確な空洞はなく、小さな細胞の塊から成ります。この段階の胚の細胞(割球)は全能性を持ち、将来の胎児と胎盤の双方になる能力があります。
受精後5日目頃までに、桑実胚の内部に胚盤腔と呼ばれる空洞ができ始め、内部細胞塊と外側の細胞層に分かれた構造が現れます (Embryology – Cellular Division – Gastrulation – TeachMeAnatomy)。これが胚盤胞(はいばんほう, blastocyst)と呼ばれる段階です。胚盤胞は内部細胞塊(胚節ともいう、将来胚そのものになる細胞群)と、外側を囲む栄養外胚葉(将来胎盤など胚を支える組織になる細胞群)に分化し始めた状態です (Embryology – Cellular Division – Gastrulation – TeachMeAnatomy)。胚盤胞まで成長した胚は、透明帯から脱出(ハッチング)して子宮内膜への着床準備を整えます。受精後およそ6日目に胚盤胞は子宮内膜へ着床(インプラント)し、母体から栄養を受け取ってさらに発生を続けます (Stages of Fetal Development – Women’s Health Issues – Merck Manual Consumer Version)。
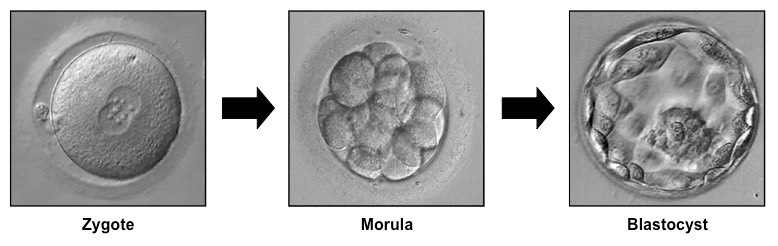
(Embryo Development | BioNinja) 図1: 受精卵(左)から桑実胚(中央)、胚盤胞(右)へと初期発生が進む様子を示す胚の模式図。受精卵は細胞分裂を繰り返し、細胞数16前後の桑実胚を経て、内部に空洞(胚盤腔)をもつ胚盤胞へと成長する(ヒトでは受精後約5日で胚盤胞に到達する)。胚盤胞では内部細胞塊(将来の胎児部分)と外周の栄養膜(将来の胎盤部分)に細胞が分かれ始めている。
体軸形成と細胞分化の仕組み
胚がさらに発生を進めると、体軸形成と呼ばれる体の基本的な方向づけが行われます。左右相称動物であるヒトの胚では、頭側と尾側を結ぶ前後軸(頭尾軸)と、背中側と腹側を区別する背腹軸がまず確立し、続いて左右の非対称性(左右軸)が決定されていきます (体軸 – Wikipedia)。たとえば脊椎動物の胚では、胚盤胞が着床した後に原始線条と呼ばれる構造が胚盤上に現れ、これが胚の頭尾方向を決める重要な合図となります (Body Axis Formation: Embryonic & Vertebrate | Vaia)。原始線条付近では形成体と呼ばれる特殊な組織が周囲の細胞にシグナルを送り、胚の各部における位置情報を与えます。胚内ではモルフォゲン(形態形成物質)と総称されるシグナル分子の濃度勾配が形成されており、この勾配によって細胞は自らの位置を「読み取り」適切な分化プログラムを実行します (Body Axis Formation: Embryonic & Vertebrate | Vaia)。こうした分子メカニズムにより、頭部から尾部、背側から腹側にかけて組織や器官の配置が統制されるのです。
左右の軸(左右非対称性)の決定も発生学上の大きな謎でしたが、そのメカニズムの一端が解明されつつあります。哺乳類では胚の節(ノード)と呼ばれる部分にある繊毛の回転運動によって胚内に左向きの液流(ノード流)が生じ、それに伴い左右差を決める遺伝子(例えば左側でのNodal遺伝子やそれによって誘導されるPitx2遺伝子)の発現が非対称に開始されます (体軸 – Wikipedia)。この結果、心臓が左、肝臓が右といった左右の臓器配置が確立されます。左右軸は他の軸よりも後に決まる軸であり (体軸 – Wikipedia)、その破綻は重篤な先天異常につながることから、現在も盛んに研究が行われている分野です。
胚の組織づくりにおいては、胚葉形成と呼ばれるもう一つの重要なイベントがあります。ヒトでは受精後2週目から3週目にかけて原腸形成(ガストリュレーション)が起こり、胚盤胞の内部細胞塊から外胚葉・中胚葉・内胚葉という三つの胚葉が作り出されます (Embryo – Wikipedia) (Embryo – Wikipedia)。これら胚葉は発生の「素材」とも言えるもので、それぞれ将来に特定の組織群へ分化します。例えば、外胚葉からは表皮や神経系の細胞が分化し、中胚葉からは骨や筋肉、血液などの組織が生じます。内胚葉からは消化管や肺などの内臓の上皮細胞が形成されます (Basic Embryology)。胚葉ごとに発現させる遺伝子のプログラムを変化させることで、細胞は自らの運命を定めていくのです。
こうした細胞分化のプロセスでは、不要となる細胞の**アポトーシス(プログラム細胞死)**も形づくりに利用されます。例えばヒトの指の間の水かきは胚発生のある段階で細胞死によって消失しますが、これは適切な形態形成の一環です。このように、細胞分裂・分化・細胞死といった現象が精妙に統御されることで、一つの受精卵から何十兆もの細胞が秩序だった一個体へと作り上げられていくのです。
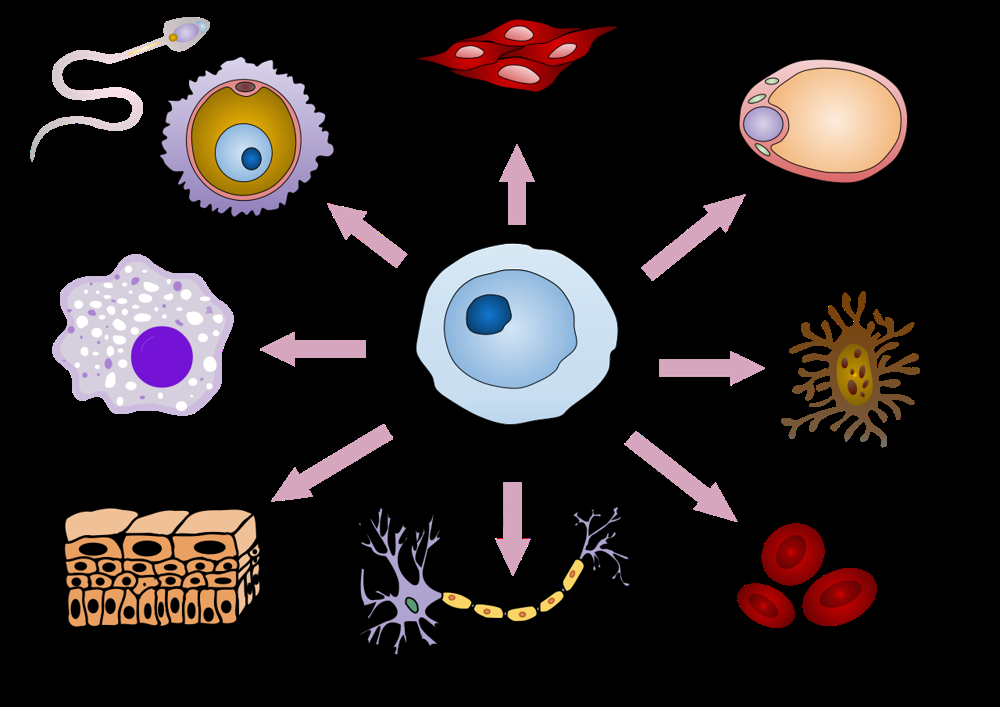
(File:Final stem cell differentiation (1).svg – Wikimedia Commons) 図2: 幹細胞(中央の水色の細胞)が様々な細胞種に分化していく概念図。中央の未分化な細胞から外側に向かって、上皮細胞(左下の細胞層)、神経細胞(下中央の樹状の細胞)、赤血球(右下の赤い細胞)など、多彩な細胞が矢印に沿って生み出されていく様子を模式的に示している。細胞分化とは、同じゲノムにも関わらず細胞によって発現する遺伝子の組み合わせが変化し、細胞が特定の形や働きをもつようになる現象である (〖高校生物基礎〗「ヒトの細胞とゲノムの働き」 | 映像授業のTry IT (トライイット))。
最新の研究動向
オルガノイド研究
近年、発生学の知見を応用したオルガノイド研究が飛躍的に進歩しています。オルガノイド(Organoid)とは培養下で幹細胞から作製されるミニ臓器のことで、その名の通り「臓器のようなもの」を意味します。オルガノイドと呼ぶためには、実際の臓器と同じように複数種類の細胞から構成され、秩序だった三次元構造を持ち、かつ臓器らしい機能を発現している必要があります (小さな臓器“オルガノイド”研究が拓く未来――新たなアイデアを生み出す思考とは | メディカルノート)。2000年代以降の幹細胞培養技術の発展により、ヒトの多能性幹細胞(ES細胞やiPS細胞)から腸や肝臓、腎臓、脳など様々なオルガノイドが作製されるようになりました。
オルガノイドは小さいながらも元の臓器に近い性質を示すため、現在では発生学や病理学の研究ツールとして盛んに利用されています。たとえば患者由来の幹細胞から病変臓器のオルガノイドを作製すれば、試験管内で病気のモデルを再現することが可能です。実際に肝臓オルガノイドを用いて難治性肝疾患の病態解明や創薬研究が進みつつあり (小さな臓器“オルガノイド”研究が拓く未来――新たなアイデアを生み出す思考とは | メディカルノート)、脳オルガノイド(ミニブレイン)を発達させてヒトの脳発生過程や神経疾患(マイクロセファリーなど)の研究に応用する試みも行われています。また、オルガノイドは患者ごとの細胞から作れるため、創薬候補物質の効果や副作用を個別化医療の観点で評価するプラットフォームとしても期待されています (What Are Organoids and How Are They Made? | The Scientist)。このようにオルガノイド研究は、発生学の知見を病気の解明や治療法の開発へと橋渡しする最先端分野です。
幹細胞研究(iPS細胞と発生学)
幹細胞とは様々な細胞に分化できる能力(多分化能)と増殖能力を持つ細胞で、発生学の研究になくてはならない存在です。中でも2006年に京都大学の山中伸弥教授らが開発した人工多能性幹細胞(iPS細胞)の技術は、発生学と再生医療に革命をもたらしました。iPS細胞とは、皮膚や血液など成体の体細胞に数種類の「初期化因子」(山中因子と呼ばれる特定の遺伝子群)を導入して初期胚のような未分化状態に巻き戻した多能性幹細胞のことです (iPS細胞の分化成熟能力を高める技術を開発|ニュース&イベント|順天堂大学) (用語説明 | もっと知るiPS細胞 | 京都大学iPS細胞研究所 CiRA(サイラ))。言い換えれば、一度分化した細胞の核を受精卵と同じような状態にリセットし、**胚性幹細胞(ES細胞)**に近い性質を持たせたものがiPS細胞です。この技術により、患者自身の細胞からあらゆる細胞に分化しうる幹細胞を樹立できるようになり、拒絶反応のない移植用細胞の作製や難病の病態解明につながる画期的な道が開かれました (iPS細胞の分化成熟能力を高める技術を開発|ニュース&イベント|順天堂大学)。
iPS細胞は発生学研究への強力なツールとなっています。従来、生体の中でしか観察できなかったヒトの組織形成過程を、試験管内で再現し研究することが可能になったためです。例えば、ヒトiPS細胞から心筋細胞や神経細胞、血液細胞などを分化誘導し、その分化の段階ごとに分子挙動を解析することで、ヒトの臓器が形作られるメカニズムや疾患発症のプロセスを詳細に調べることができます。また患者由来のiPS細胞から目的の細胞を作り出せば、病気の「発生過程」をモデル化して薬剤効果を試すこともできます (iPS細胞の分化成熟能力を高める技術を開発|ニュース&イベント|順天堂大学)。こうした研究は、発生学の知識を発展させると共に、再生医療や創薬にも直結するものです。実際、iPS細胞を用いた網膜や心筋への細胞移植治験が進むなど再生医療は着実に成果を上げつつあり、これは発生学的原理の応用による一例と言えます。
クローン技術
最後に、クローン技術についても発生学と深い関わりがあります。クローン技術とは、ある個体と全く同じ遺伝情報を持つ個体(クローン)を作り出す技術です。中でも1996年にイギリスで誕生したクローン羊「ドリー」は有名で、これは成体の乳腺細胞から取り出した核を核を除去した未受精卵に移植し、その卵を代理母に着床させて生まれた世界初の哺乳類クローンです (ドリー (羊) – Wikipedia)。ドリーの作製には体細胞核移植(SCNT)という発生工学的手法が用いられましたが、ドリーの誕生は「分化した細胞の核にも、依然として一個体を形成するための全遺伝情報(設計図)が含まれている」ことを実証し、生命科学に大きなインパクトを与えました。つまり、発生学の原理に従えば、特殊化した細胞も適切な環境下(未受精卵の中)では受精卵のように振る舞い、そこから新たな個体へと発生をやり直すことが可能であると示されたのです。
しかし、ドリーの誕生は同時にクローン技術に関する激しい倫理論争も引き起こしました。人為的にクローン生物を作り出すことへの社会的な不安や抵抗感は大きく、多くの人々が「あらゆる形のクローン生物の産生は倫理的に誤っており禁止すべきだ」と主張するようになりました (ドリー (羊) – Wikipedia)。その結果、各国でヒトクローン胚の作成・出産を禁止する法律が整備され、日本においても2001年に「ヒトに関するクローン技術の規制に関する法律」が施行されています。また、クローン動物には寿命や健康への影響(例えばドリーのテロメア短縮問題)も指摘されており、技術の安全性にも課題が残ります。一方でクローン技術自体は年々進歩を遂げており、ドリー以降もウシやブタ、サルなど多くの哺乳類でクローン個体の作製に成功しています (ドリー (羊) – Wikipedia)。将来的にはこの技術を応用して、絶滅の危機に瀕した動物種の保全や、優良な家畜・ペットのクローン作製といった分野への応用も模索されています (ドリー (羊) – Wikipedia)。クローン技術の発展は発生学の理解と表裏一体であり、その適切な利用については今後も慎重な議論が求められるでしょう。
まとめ
受精卵から一個の個体が形作られるまでの過程は、生命科学における最大の謎の一つです。発生学の研究を通じて、この神秘的なプロセスの分子メカニズムが次第に明らかになりつつありますが、未だ解明されていないことも多く残されています。昨今のオルガノイドや幹細胞、ゲノム編集などの新技術により、発生学は毎年のように教科書を書き換える勢いで進歩している分野でもあります。今後、発生学の知見は再生医療や先天性疾患の治療、不妊治療の改善、畜産や野生生物保全など幅広い領域で応用され、人類に大きな利益をもたらすと期待されています。生命の設計図を読み解く発生学の研究は、生命の根源を探る純粋科学であると同時に、未来の医療とテクノロジーを支える基盤として、その重要性を増していくことでしょう。
参考文献: 発生学の基本概念および初期発生 (Basic Embryology) (Basic Embryology)、受精から胚盤胞までの過程 (Embryology – Cellular Division – Gastrulation – TeachMeAnatomy) (Embryology – Cellular Division – Gastrulation – TeachMeAnatomy) (Embryology – Cellular Division – Gastrulation – TeachMeAnatomy) (桑実胚(そうじつはい)とは? 意味や使い方 – コトバンク) (Stages of Fetal Development – Women’s Health Issues – Merck Manual Consumer Version)、体軸形成のメカニズム (体軸 – Wikipedia) (Body Axis Formation: Embryonic & Vertebrate | Vaia) (Body Axis Formation: Embryonic & Vertebrate | Vaia) (体軸 – Wikipedia)、胚葉形成と分化 (Embryo – Wikipedia) (Basic Embryology) (〖高校生物基礎〗「ヒトの細胞とゲノムの働き」 | 映像授業のTry IT (トライイット))、オルガノイド研究 (小さな臓器“オルガノイド”研究が拓く未来――新たなアイデアを生み出す思考とは | メディカルノート) (小さな臓器“オルガノイド”研究が拓く未来――新たなアイデアを生み出す思考とは | メディカルノート) (What Are Organoids and How Are They Made? | The Scientist)、iPS細胞と発生学 (iPS細胞の分化成熟能力を高める技術を開発|ニュース&イベント|順天堂大学) (用語説明 | もっと知るiPS細胞 | 京都大学iPS細胞研究所 CiRA(サイラ)) (iPS細胞の分化成熟能力を高める技術を開発|ニュース&イベント|順天堂大学)、クローン技術 (ドリー (羊) – Wikipedia) (ドリー (羊) – Wikipedia) (ドリー (羊) – Wikipedia)。